-
Atomic-scale and close-to-atomic scale manufacturing, a frontier hot issue in international academic research, is a cutting-edge manufacturing technique in which atoms are directly used as the manipulation object and atomic-scale structures with specific functions are established to meet the requirements for mass productions. This review focuses on precise atomic-scale manufacturing technology of nucleic acid materials. Firstly, the basic structures and functions of nucleic acid materials are introduced, and the basic principles of the interaction between DNA and metal atoms are discussed. Then the development process and breakthrough progress of nucleic acid materials-mediated precise atomic-scale manufacturing are introduced from the aspects of natural nucleic acid materials, artificial base “molecular elements”, and nucleic acid nanostructures. Finally, the challenges and opportunities in this field are systematically summarized and some suggestions for future development are given.
-
Keywords:
- atomic manufacturing /
- nucleic acid materials /
- metal atoms /
- precision assembly
[1] 房丰洲 2020 中国机械工程 31 1009
 Google Scholar
Google Scholar
Fang F 2020 Chinese Mech. Eng. 31 1009
 Google Scholar
Google Scholar
[2] 李沫, 李倩, 张健 2016 太赫兹科学与电子信息学报 14 793
 Google Scholar
Google Scholar
Li M, Li Q, Zhang J 2016 J. Terahertz Sci. Electron. Inf. Technol. 14 793
 Google Scholar
Google Scholar
[3] Jiang D, England C G, Cai W 2016 J. Control. Release 239 27
 Google Scholar
Google Scholar
[4] Dai Z, Leung H M, Lo P K 2017 Small 13 1602881
 Google Scholar
Google Scholar
[5] Lippert B 2000 Coord. Chem. Rev. 200 487
 Google Scholar
Google Scholar
[6] Morris D L 2014 Biomol. Concepts 5 397
 Google Scholar
Google Scholar
[7] Liu J, Lu Y 2004 J. Am. Chem. Soc. 126 12298
 Google Scholar
Google Scholar
[8] Cai W, Xie S, Zhang J, Tang D, Tang Y 2018 Biosens. Bioelectron. 117 3128
 Google Scholar
Google Scholar
[9] Jia X, Li J, Han L, Ren J, Yang X, Wang E 2012 ACS Nano 6 3311
 Google Scholar
Google Scholar
[10] Chen A, Ma S, Zhuo Y, Chai Y, Yuan R 2016 Anal. Chem. 88 3203
 Google Scholar
Google Scholar
[11] Fu J, Zhang Z, Li G 2019 Chinese Chem. Let. 30 285
 Google Scholar
Google Scholar
[12] Wagenknecht H A 2003 Angew. Chem. Int. Ed. 42 3204
 Google Scholar
Google Scholar
[13] Wheate N J, Walker S, Craig G E, Oun R 2010 Dalton Trans. 39 8113
 Google Scholar
Google Scholar
[14] Erxleben A 2017 CHIMIA 71 102
 Google Scholar
Google Scholar
[15] Belmont P, Constan, J F, Demeunynck M 2001 Chem. Soc. Rev. 30 70
 Google Scholar
Google Scholar
[16] Shamsi M H, Kraatz H B 2013 J. Inorg. Organomet. Polym. Mater. 23 4
 Google Scholar
Google Scholar
[17] Sigel H 1993 Chem. Soc. Rev. 22 255
 Google Scholar
Google Scholar
[18] Pages B J, Ang D L, Wright E P, Aldrich-Wright J R 2015 Dalton Trans. 44 3505
 Google Scholar
Google Scholar
[19] Müller J 2010 Metallomics 2 318
 Google Scholar
Google Scholar
[20] Kellett A, Molphy Z, Slator C, McKee V, Farrell N P 2019 Chem. Soc. Rev. 48 971
 Google Scholar
Google Scholar
[21] Ono A, Togashi H 2004 Angew. Chem. 116 4400
 Google Scholar
Google Scholar
[22] Jiang X, Wang H, Wang H, Yuan R, Chai Y 2016 Anal. Chem. 88 9243
 Google Scholar
Google Scholar
[23] Zhang B, Guo L H 2012 Biosens. Bioelectron. 37 112
 Google Scholar
Google Scholar
[24] Huang J, Gao X, Jia J, Kim J K, Li Z 2014 Anal. Chem. 86 3209
 Google Scholar
Google Scholar
[25] Ono A, Cao S, Togashi H, Tashiro M, Fujimoto T, Machinami T, Oda S, Miyake Y, Okamato I, Tanaka Y 2008 Chem. Commun. 39 4825
 Google Scholar
Google Scholar
[26] Zhao C, Qu K, Song Y, Xu C, Ren J, Qu X 2010 Chem. Eur. J. 16 8147
 Google Scholar
Google Scholar
[27] Zheng Y, Yang C, Yang F, Yang X 2014 Anal. Chem. 86 3849
 Google Scholar
Google Scholar
[28] Park S, Sugiyama H 2010 Angew. Chem. Int. Ed. 49 3870
 Google Scholar
Google Scholar
[29] Wang C, Li Y, Jia G, Liu Y, Lu S, Li C 2012 Chem. Commun. 48 6232
 Google Scholar
Google Scholar
[30] Cepeda V, Fuertes M A, Castilla J, Alonso C, Quevedo C, Perez J M 2007 Anti-Cancer. Agents Med. Chem. 7 3
 Google Scholar
Google Scholar
[31] Wang D, Lippard S J 2005 Nat. Rev. Drug Discovery 4 307
 Google Scholar
Google Scholar
[32] Hartinger C G, Zorbas-Seifried S, Jakupec M A, Kynast B, Zorbas H, Keppler B K 2006 J. Inorg. Biochem. 100 891
 Google Scholar
Google Scholar
[33] Komor A C, Barton J K 2013 Chem. Commun. 49 3617
 Google Scholar
Google Scholar
[34] Wu T, Liu J, Liu M, Liu S, Zhao S. Tian R, Wei D, Liu Y, Zhao Y, Xiao H, Ding B 2019 Angew. Chem. In. Ed. 58 14224
 Google Scholar
Google Scholar
[35] Chen Y. Xu J, Su J, Xiang Y, Yuan R, Chai Y 2012 Anal. Chem. 84 7750
 Google Scholar
Google Scholar
[36] Wang H, Yuan Y, Zhuo Y, Chai Y, Yuan R 2016 Anal. Chem. 88 5797
 Google Scholar
Google Scholar
[37] Li S K, Chen A Y, Chai Y Q, Yuan R, Zhuo Y 2016 Electrochim. Acta 212 767
 Google Scholar
Google Scholar
[38] Kosman J, Juskowiak B 2011 Anal. Chim. Acta 707 7
 Google Scholar
Google Scholar
[39] Yang X, Li T, Li B, Wang E 2010 Analyst 135 71
 Google Scholar
Google Scholar
[40] Huang R, He L, Xia Y, Xu H, Liu C, Xie H, Wang S, Peng Li, Liu Y, Liu Y, He N, Li Z 2019 Small 15 1900735
 Google Scholar
Google Scholar
[41] Golub E, Freeman R, Willner I 2011 Angew. Chem. 123 11914
 Google Scholar
Google Scholar
[42] Chen Y, Phipps M L, Werner J H, Chakraborty S, Martinez J S 2018 Accounts Chem. Res. 51 2756
 Google Scholar
Google Scholar
[43] Petty J T, Zheng J, Hud N V, Dickson R M 2004 J. Am. Chem. Soc. 126 5207
 Google Scholar
Google Scholar
[44] Sharma J, Yeh H C, Yoo H, Werner J H, Martinez J S 2010 Chem. Commun. 46 3280
 Google Scholar
Google Scholar
[45] Lan G Y, Chen W Y, Chang H T 2011 RSC Adv. 1 802
 Google Scholar
Google Scholar
[46] Gwinn E G, O'Neill P, Guerrero A J, Bouwmeester D, Fygenson D K 2008 Adv. Mater. 20 279
 Google Scholar
Google Scholar
[47] Feng L, Huang Z, Ren J, Qu X 2012 Nucleic Acids Res. 40 e122
 Google Scholar
Google Scholar
[48] Liu Y Q, Zhang M, Yin B C, Ye B C 2012 Anal. Chem. 84 5165
 Google Scholar
Google Scholar
[49] Liu J J, Song X R, Wang Y W, Zheng A X, Chen G N, Yang H H 2012 Anal. Chim. Acta 749 70
 Google Scholar
Google Scholar
[50] Lyu D, Li J, Wang X, Guo W, Wang E 2018 Anal. Chem. 91 2050
 Google Scholar
Google Scholar
[51] Thomas A C 2012 Chem. Commun. 48 6845
 Google Scholar
Google Scholar
[52] Qing Z, He X, He D, Wang K, Xu F, Qing T, Yang X 2013 Angew. Chem. In. Ed. 52 9719
 Google Scholar
Google Scholar
[53] Zhou F, Cui X, Shang A, Lian J, Yang L, Jin Y, Li B 2017 Microchim. Acta 184 773
 Google Scholar
Google Scholar
[54] Ai J, Guo W, Li B, Li T, Li D, Wang E 2012 Talanta 88 450
 Google Scholar
Google Scholar
[55] Fu Y, Zhao X, Zhang J, Li W 2014 J. Phys. Chem. C 118 18116
 Google Scholar
Google Scholar
[56] Li W, Li W, Hu Y, Xia Y, Shen Q, Nie Z, Huang Y, Yao S 2013 Biosen. Bioelectron. 47 345
 Google Scholar
Google Scholar
[57] Wu L L, Wang L Y, Xie Z J, Pan N, Peng C F 2016 Sens. Actuators, B 235 110
 Google Scholar
Google Scholar
[58] Navani N K, Li Y 2006 Curr. Opin. Chem. Biol. 10 272
 Google Scholar
Google Scholar
[59] Stoltenburg R, Reinemann C, Strehlitz B 2007 Biomol. Eng. 24 381
 Google Scholar
Google Scholar
[60] Zhan S, Wu Y, Wang L, Zhan X, Zhou P 2016 Biosens Bioelectron. 86 353
 Google Scholar
Google Scholar
[61] Dass C R, Choong P F, Khachigian L M 2008 Mol. Cancer Ther. 7 243
 Google Scholar
Google Scholar
[62] McGhee C E, Loh K Y, Lu Y 2017 Curr. Opin. Biotechnol. 45 191
 Google Scholar
Google Scholar
[63] Fan H, Zhang X, Lu Y 2017 Sci. China Chem. 60 591
 Google Scholar
Google Scholar
[64] Li L, Xu S, Yan H, Li X, Yazd H S, Li X, Huang T, Cui C, Jiang J, Tan W 2020 Angew. Chem. Int. Ed. 59 2
 Google Scholar
Google Scholar
[65] Pang X, Cui C, Wan S., Jiang Y, Zhang L, Xia L, Li L, Li X, Tan W 2018 Cancers 10 47
 Google Scholar
Google Scholar
[66] Meng H M, Liu H, Kuai H, Peng R, Mo L, Zhang X B 2016 Chem. Soc. Rev. 45 2583
 Google Scholar
Google Scholar
[67] Li S, Xu J, Wang S, Xia X, Chen L, Chen Z 2019 Chinese Chem. Lett. 30 1581
 Google Scholar
Google Scholar
[68] Zhang D, Yin L, Meng Z, Yu A, Guo L, Wang H 2014 Anal. Chim. Acta 812 161
 Google Scholar
Google Scholar
[69] Lei Y M, Huang W X, Zhao M, Chai Y Q, Yuan R, Zhuo Y 2015 Anal. Chem. 87 7787
[70] 陈俊俊, 李称, 徐斐, 曹慧, 叶泰, 于劲松, 袁敏 2018 工业微生物 3 11
 Google Scholar
Google Scholar
Chen J J, Li C, Xu F, Cao H, Ye T, Y u, J S, Yuan M 2018 Industrial Microorganisms 3 11
 Google Scholar
Google Scholar
[71] Williamson J R 1994 Annu. Rev. Bioph. Biom. 23 703
 Google Scholar
Google Scholar
[72] Chung C H, Kim J H, Jung J, Chung B H 2013 Biosen. Bioelectron. 41 827
 Google Scholar
Google Scholar
[73] Peng Y, Li Y, Li L, Zhu J J 2018 J. Hazard. Mater. 359 121
 Google Scholar
Google Scholar
[74] Breaker R R, Joyce G F 1994 Chem. Biol. 1 223
 Google Scholar
Google Scholar
[75] Ihms H E, Lu Y 2012 Humana Press 848 297
 Google Scholar
Google Scholar
[76] Liang W B, Zhuo Y, Zheng Y N, Xiong C Y, Chai Y Q, Yuan R 2017 ACS Appl. Mater. Interfaces 9 39812
 Google Scholar
Google Scholar
[77] Hong C, Kim D M, Baek A, Chung H, Jung W, Kim D E 2015 Chem. Commun. 51 5641
 Google Scholar
Google Scholar
[78] Chen J, Zuehlke A, Deng B, Peng H, Hou X, Zhang H 2017 Anal. Chem. 89 12888
 Google Scholar
Google Scholar
[79] Fan H, Zhao Z, Yan G, Zhang X, Yang C, Meng H, Chen Z, Liu H, Tan W 2015 Angew. Chem. 127 4883
 Google Scholar
Google Scholar
[80] Wang H, Wang H, Wu Q, Liang M, Liu X, Wang F 2019 Chem. Sci. 10 9597
 Google Scholar
Google Scholar
[81] Khakshoor O, Kool E T 2011 Chem. Commun. 47 7018
 Google Scholar
Google Scholar
[82] Pinheiro V B, Holliger P 2012 Curr. Opin. Chem. Biol. 16 245
 Google Scholar
Google Scholar
[83] Nielsen P E, Haaima G 1997 Chem. Soc. Rev. 26 73
 Google Scholar
Google Scholar
[84] Corradini R, Sforza S, Tedeschi T, Totsingan F, Manicardi A, Marchelli R 2011 Curr. Top. Med. Chem. 11 1535
 Google Scholar
Google Scholar
[85] Whittell G R, Manners I 2007 Adv. Mater. 19 3439
 Google Scholar
Google Scholar
[86] James H R 2012 Chem. Commun. 48 12165
 Google Scholar
Google Scholar
[87] Clever G H, Shionoya M 2010 Coord. Chem. Rev. 254 2391
 Google Scholar
Google Scholar
[88] Johannsen S, Megger N, Böhme D, Sige R K, Mn F, Manicard Nat. Chem. 2 229
[89] Zhu T, Wu Q, Chen P, Ding Y 2009 J. Organomet. Chem. 694 21
 Google Scholar
Google Scholar
[90] Li D, Song S, Fan C 2010 Accounts Chem. Res. 43 631
 Google Scholar
Google Scholar
[91] Abdullah R, Xie S, Wang R, Jin C, Du Y, Fu T, Li J, Zhang L, Tan W 2018 Anal. Chem. 91 2074
 Google Scholar
Google Scholar
[92] Wang R, Zhu G, Mei L, Xie Y, Ma H, Ye M, Qing F L, Tan W 2014 J. Am. Chem. Soc. 136 2731
 Google Scholar
Google Scholar
[93] Jin C, Liu X, Bai H, Wang R, Tan J, Peng X, Tan W 2017 ACS Nano 11 12087
 Google Scholar
Google Scholar
[94] Jin C, He J, Zou J, Xuan W, Fu T, Wang R, Tan W 2019 Nat. Commun. 10 2704
 Google Scholar
Google Scholar
[95] Xie S, Qiu L, Cui L, Liu H, Sun Y, Liang H, Ding D, He L, Liu H, Zhang J, Chen, Z. Zhang X, Tan W 2017 Chem 3 1021
 Google Scholar
Google Scholar
[96] Tan J, Li H, Hu X, Abdullah R, Xie S, Zhang L, Zhao M, Luo Q, Li Y, Sun Z, Yuan Q, Tan W 2019 Chem 5 1775
 Google Scholar
Google Scholar
[97] Zhang L, Abdullah R, H X, Bai H, Fan H, He L, Liang H, Zou J, Liu Y, Zhang, X. Tan W 2019 J. Am. Chem. Soc. 141 4282
 Google Scholar
Google Scholar
[98] Kallenbach N R, Ma R I, Seeman N C 1983 Nature 305 829
 Google Scholar
Google Scholar
[99] Seeman N C 2003 Nature 421 427
 Google Scholar
Google Scholar
[100] Aldaye F A, Palmer A L, Sleiman H F 2008 Science 321 1795
 Google Scholar
Google Scholar
[101] Seeman N C 2010 Annu. Rev. Biochem. 79 6
 Google Scholar
Google Scholar
[102] Wang Z G, Ding B 2014 Accounts Chem. Res. 47 1654
 Google Scholar
Google Scholar
[103] Veneziano R, Moyer T J, Stone M B, Wamhoff E C, Read B J, Mukherjee S, Shepherd T R, Das J, Schief W R, Irvine D J, Bathe M 2020 Nat. Nanotechnol. 15 716
 Google Scholar
Google Scholar
[104] He X, Dong L, Wang W, Lin N, Mi Y 2013 Chem. Commun. 49 2906
 Google Scholar
Google Scholar
[105] Liu Y, Chen Q, Liu J, Yang X, Guo Q, Li L, Liu W, Wang K 2017 Anal. Chem. 89 3590
 Google Scholar
Google Scholar
[106] Ke Y, Sharma J, Liu M, Jahn K, Liu Y, Yan H 2009 Nano Lett. 9 2445
 Google Scholar
Google Scholar
[107] Sadowski J P, Calvert C R, Zhang D Y, Pierce N A, Yin P 2014 ACS Nano 8 3251
 Google Scholar
Google Scholar
[108] Mou Q, Ma Y, Pan G, Xue B, Yan D, Zhang C, Zhu X 2017 Angew. Chem. 129 12702
 Google Scholar
Google Scholar
[109] Shiu S C C, Fraser L A, Ding Y, Tanner J A 2018 Molecules 23 1695
 Google Scholar
Google Scholar
[110] Um S H, Lee J B, Park N, Kwon, S Y, Umbach C C, Luo D 2006 Nat. Mater. 5 797
 Google Scholar
Google Scholar
[111] Shahbazi M A, Baulethk N, Kwon, S Y, Umbach C C Adv. Therap. 1 1800042
[112] He Y, Tian Y, Chen Y, Deng Z, Ribbe A E, Mao C 2005 Angew. Chem. Int. Ed. 44 6694
 Google Scholar
Google Scholar
[113] He Y, Chen Y, Liu H, Ribbe A E, Mao C 2005 J. Am. Chem. Soc. 127 12202
 Google Scholar
Google Scholar
[114] Douglas S M, Marblestone A H, Teerapittayanon S, Vazquez A, Church G M, Shih W M 2009 Nucleic Acids Res. 37 5001
 Google Scholar
Google Scholar
[115] Bila H, Kurisinkal E E, Bastings M M 2019 Biomater. Sci. 7 532
 Google Scholar
Google Scholar
[116] Rothemund P W K 2006 Nature 440 297
 Google Scholar
Google Scholar
[117] Veneziano R, Ratanalert S, Zhang K, Zhang F, Yan H, Chiu W, Bathe M 2016 Science 352 1534
 Google Scholar
Google Scholar
[118] Schreiber R, Do J, Roller E M, Zhang T, Sch, ler, V J, Nickels P C, Feldmann J, Liedl T 2014 Nat. Nanotechnol. 9 74
 Google Scholar
Google Scholar
[119] Zhan P, Wen T, Wang Z G, He Y, Shi J, Wang T. Liu X, Lu G, Ding B 2018 Angew. Chem. Int. Ed. 57 2846
 Google Scholar
Google Scholar
[120] Ding B, Deng Z, Yan H, Cabrini S, Zuckermann R N, Bokor J 2010 J. Am. Chem. Soc. 132 3248
 Google Scholar
Google Scholar
[121] Tian Y, Wang T, Liu W, Xin H L, Li H, Ke Y, M. Shih W, Gang O 2015 Nat. Nanotechnol. 10 637
 Google Scholar
Google Scholar
[122] Jia S, Wang J, Xie M, Sun J, Liu H, Zhang Y, Chao J, Li J, Wang L, Lin J, Gothelf K V, Fan C 2019 Nat. Commun. 10 5597
 Google Scholar
Google Scholar
[123] Liu X, Zhang F, Jing X, Pan M, Liu P, Li W, Zhu B, Li J, Chen H, Wang L, Lin J, Liu Y, Zhao D, Yan H, Fan C 2018 Nature 559 593
 Google Scholar
Google Scholar
[124] Schreiber R, Luong N, Fan, Z, Kuzyk A, Nickels P C, Zhang T, Smith D M, Yurke B, Kuang W, Govorov A O, Liedl T 2013 Nat. Commun. 4 1
 Google Scholar
Google Scholar
[125] Urban M J, Dutta P K, Wang P, Duan, X, Shen X, Ding B, Ke Y, Liu N 2016 J. Am. Chem. Soc. 138 5495
 Google Scholar
Google Scholar
[126] Wang P, Meyer T A, Pan V, Dutta P K, Ke Y 2017 Chem 2 359
 Google Scholar
Google Scholar
[127] Loretan M, Domljanovic I, Lakatos M, Re Y 2017 Ding B, Ke Y Materials 13 2185
 Google Scholar
Google Scholar
[128] Fu J, Liu M, Liu Y, Woodbury N W, Yan H 2012 J. Am. Chem. Soc. 134 5516
 Google Scholar
Google Scholar
[129] Liu N, Dai M, Saka S K, Yin P 2019 Nat. Chem. 11 1001
 Google Scholar
Google Scholar
[130] Braun E, Eichen Y, Sivan U, Ben-Yoseph G 1998 Nature 391 775
 Google Scholar
Google Scholar
[131] Liu J, Geng Y, Pound E, Gyawali S, Ashton J R, Hickey J, Woolley A T, Harb J N 2011 ACS Nano 5 2240
 Google Scholar
Google Scholar
[132] Geng Y, Liu J, Pound E, Gyawali S, Harb J N, Woolley A T 2011 J. Mater. Chem. 21 12126
 Google Scholar
Google Scholar
[133] Geng Y, Pearson A C, Gates E P, Uprety B, Davis R C, Harb J N, Woolley A T 2013 Langmuir 29 3482
 Google Scholar
Google Scholar
[134] Pilo-Pais M, Goldberg S, Samano E, LaBean T H, Finkelstein G 2011 Nano Lett. 11 3489
 Google Scholar
Google Scholar
[135] Helmi S, Ziegler C, Kauert D J, Seidel R 2014 Nano Lett. 14 6693
 Google Scholar
Google Scholar
[136] Sun W, Boulais E, Hakobyan Y, Wang W L, Guan A, Bathe M, Yin P 2014 Science 346 6210
 Google Scholar
Google Scholar
-
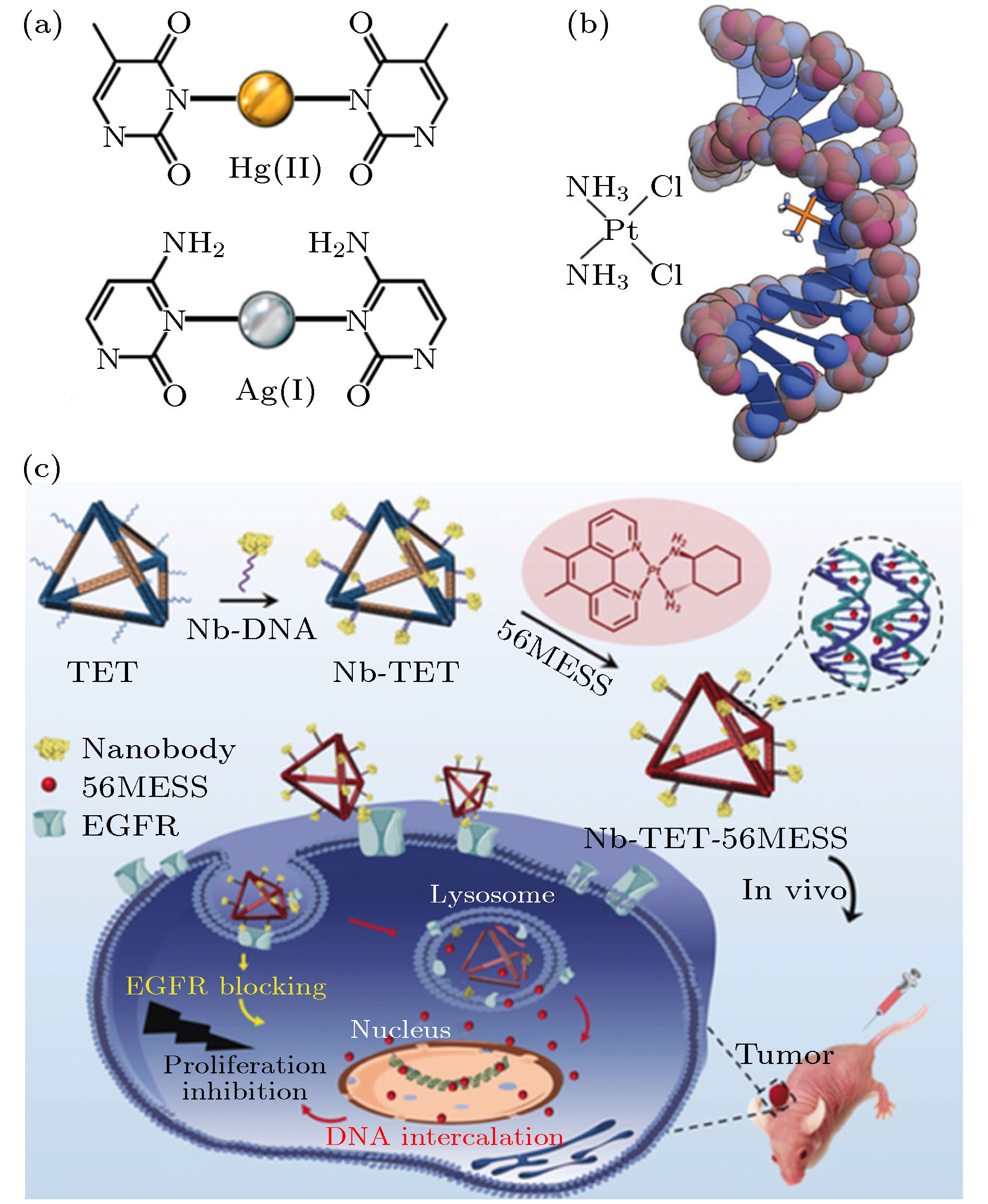
图 3 (a) T-Hg2+-T和C-Ag+-C结构示意图; (b) 顺铂与DNA相互作用形成的1, 2-链内加合物[18]; (c) 用于铂药物靶向递送的纳米抗体偶联DNA纳米平台示意图[34]
Fig. 3. (a) Illustration of T-Hg2+-T and C-Ag+-C complexes induced fluorescence quenching; (b) 1, 2-intrastrand adducts formed between cisplatin and DNA[18]; (c) illustration of a nanobody-conjugated DNA nanoplatform for targeted platinum drug delivery[34].
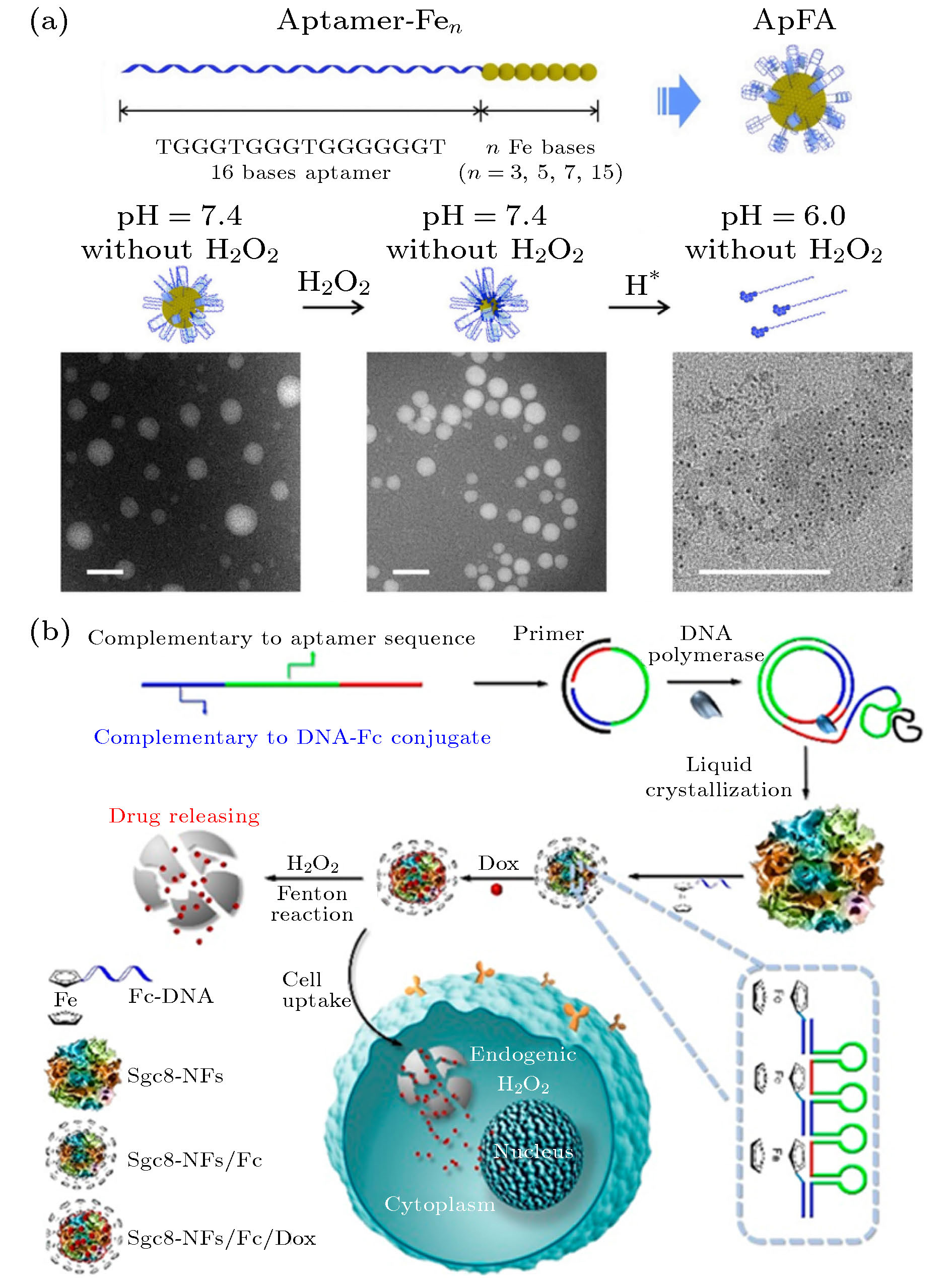
图 7 (a) 适体-Fen两亲分子的示意图以及在不同条件下的ApFAs的TEM图像[96]; (b) DOX/Sgc8-NFs-Fc的制备及其通过类芬顿反应在癌细胞中的自降解过程[97]
Fig. 7. (a) Schematic of aptamer-Fen amphiphilic molecules and TEM images of ApFAs at different conditions[96]; (b) preparation of DOX/Sgc8-NFs-Fc and its autodegradation process in cancer cells through Fenton-like reaction[97].
-
[1] 房丰洲 2020 中国机械工程 31 1009
 Google Scholar
Google Scholar
Fang F 2020 Chinese Mech. Eng. 31 1009
 Google Scholar
Google Scholar
[2] 李沫, 李倩, 张健 2016 太赫兹科学与电子信息学报 14 793
 Google Scholar
Google Scholar
Li M, Li Q, Zhang J 2016 J. Terahertz Sci. Electron. Inf. Technol. 14 793
 Google Scholar
Google Scholar
[3] Jiang D, England C G, Cai W 2016 J. Control. Release 239 27
 Google Scholar
Google Scholar
[4] Dai Z, Leung H M, Lo P K 2017 Small 13 1602881
 Google Scholar
Google Scholar
[5] Lippert B 2000 Coord. Chem. Rev. 200 487
 Google Scholar
Google Scholar
[6] Morris D L 2014 Biomol. Concepts 5 397
 Google Scholar
Google Scholar
[7] Liu J, Lu Y 2004 J. Am. Chem. Soc. 126 12298
 Google Scholar
Google Scholar
[8] Cai W, Xie S, Zhang J, Tang D, Tang Y 2018 Biosens. Bioelectron. 117 3128
 Google Scholar
Google Scholar
[9] Jia X, Li J, Han L, Ren J, Yang X, Wang E 2012 ACS Nano 6 3311
 Google Scholar
Google Scholar
[10] Chen A, Ma S, Zhuo Y, Chai Y, Yuan R 2016 Anal. Chem. 88 3203
 Google Scholar
Google Scholar
[11] Fu J, Zhang Z, Li G 2019 Chinese Chem. Let. 30 285
 Google Scholar
Google Scholar
[12] Wagenknecht H A 2003 Angew. Chem. Int. Ed. 42 3204
 Google Scholar
Google Scholar
[13] Wheate N J, Walker S, Craig G E, Oun R 2010 Dalton Trans. 39 8113
 Google Scholar
Google Scholar
[14] Erxleben A 2017 CHIMIA 71 102
 Google Scholar
Google Scholar
[15] Belmont P, Constan, J F, Demeunynck M 2001 Chem. Soc. Rev. 30 70
 Google Scholar
Google Scholar
[16] Shamsi M H, Kraatz H B 2013 J. Inorg. Organomet. Polym. Mater. 23 4
 Google Scholar
Google Scholar
[17] Sigel H 1993 Chem. Soc. Rev. 22 255
 Google Scholar
Google Scholar
[18] Pages B J, Ang D L, Wright E P, Aldrich-Wright J R 2015 Dalton Trans. 44 3505
 Google Scholar
Google Scholar
[19] Müller J 2010 Metallomics 2 318
 Google Scholar
Google Scholar
[20] Kellett A, Molphy Z, Slator C, McKee V, Farrell N P 2019 Chem. Soc. Rev. 48 971
 Google Scholar
Google Scholar
[21] Ono A, Togashi H 2004 Angew. Chem. 116 4400
 Google Scholar
Google Scholar
[22] Jiang X, Wang H, Wang H, Yuan R, Chai Y 2016 Anal. Chem. 88 9243
 Google Scholar
Google Scholar
[23] Zhang B, Guo L H 2012 Biosens. Bioelectron. 37 112
 Google Scholar
Google Scholar
[24] Huang J, Gao X, Jia J, Kim J K, Li Z 2014 Anal. Chem. 86 3209
 Google Scholar
Google Scholar
[25] Ono A, Cao S, Togashi H, Tashiro M, Fujimoto T, Machinami T, Oda S, Miyake Y, Okamato I, Tanaka Y 2008 Chem. Commun. 39 4825
 Google Scholar
Google Scholar
[26] Zhao C, Qu K, Song Y, Xu C, Ren J, Qu X 2010 Chem. Eur. J. 16 8147
 Google Scholar
Google Scholar
[27] Zheng Y, Yang C, Yang F, Yang X 2014 Anal. Chem. 86 3849
 Google Scholar
Google Scholar
[28] Park S, Sugiyama H 2010 Angew. Chem. Int. Ed. 49 3870
 Google Scholar
Google Scholar
[29] Wang C, Li Y, Jia G, Liu Y, Lu S, Li C 2012 Chem. Commun. 48 6232
 Google Scholar
Google Scholar
[30] Cepeda V, Fuertes M A, Castilla J, Alonso C, Quevedo C, Perez J M 2007 Anti-Cancer. Agents Med. Chem. 7 3
 Google Scholar
Google Scholar
[31] Wang D, Lippard S J 2005 Nat. Rev. Drug Discovery 4 307
 Google Scholar
Google Scholar
[32] Hartinger C G, Zorbas-Seifried S, Jakupec M A, Kynast B, Zorbas H, Keppler B K 2006 J. Inorg. Biochem. 100 891
 Google Scholar
Google Scholar
[33] Komor A C, Barton J K 2013 Chem. Commun. 49 3617
 Google Scholar
Google Scholar
[34] Wu T, Liu J, Liu M, Liu S, Zhao S. Tian R, Wei D, Liu Y, Zhao Y, Xiao H, Ding B 2019 Angew. Chem. In. Ed. 58 14224
 Google Scholar
Google Scholar
[35] Chen Y. Xu J, Su J, Xiang Y, Yuan R, Chai Y 2012 Anal. Chem. 84 7750
 Google Scholar
Google Scholar
[36] Wang H, Yuan Y, Zhuo Y, Chai Y, Yuan R 2016 Anal. Chem. 88 5797
 Google Scholar
Google Scholar
[37] Li S K, Chen A Y, Chai Y Q, Yuan R, Zhuo Y 2016 Electrochim. Acta 212 767
 Google Scholar
Google Scholar
[38] Kosman J, Juskowiak B 2011 Anal. Chim. Acta 707 7
 Google Scholar
Google Scholar
[39] Yang X, Li T, Li B, Wang E 2010 Analyst 135 71
 Google Scholar
Google Scholar
[40] Huang R, He L, Xia Y, Xu H, Liu C, Xie H, Wang S, Peng Li, Liu Y, Liu Y, He N, Li Z 2019 Small 15 1900735
 Google Scholar
Google Scholar
[41] Golub E, Freeman R, Willner I 2011 Angew. Chem. 123 11914
 Google Scholar
Google Scholar
[42] Chen Y, Phipps M L, Werner J H, Chakraborty S, Martinez J S 2018 Accounts Chem. Res. 51 2756
 Google Scholar
Google Scholar
[43] Petty J T, Zheng J, Hud N V, Dickson R M 2004 J. Am. Chem. Soc. 126 5207
 Google Scholar
Google Scholar
[44] Sharma J, Yeh H C, Yoo H, Werner J H, Martinez J S 2010 Chem. Commun. 46 3280
 Google Scholar
Google Scholar
[45] Lan G Y, Chen W Y, Chang H T 2011 RSC Adv. 1 802
 Google Scholar
Google Scholar
[46] Gwinn E G, O'Neill P, Guerrero A J, Bouwmeester D, Fygenson D K 2008 Adv. Mater. 20 279
 Google Scholar
Google Scholar
[47] Feng L, Huang Z, Ren J, Qu X 2012 Nucleic Acids Res. 40 e122
 Google Scholar
Google Scholar
[48] Liu Y Q, Zhang M, Yin B C, Ye B C 2012 Anal. Chem. 84 5165
 Google Scholar
Google Scholar
[49] Liu J J, Song X R, Wang Y W, Zheng A X, Chen G N, Yang H H 2012 Anal. Chim. Acta 749 70
 Google Scholar
Google Scholar
[50] Lyu D, Li J, Wang X, Guo W, Wang E 2018 Anal. Chem. 91 2050
 Google Scholar
Google Scholar
[51] Thomas A C 2012 Chem. Commun. 48 6845
 Google Scholar
Google Scholar
[52] Qing Z, He X, He D, Wang K, Xu F, Qing T, Yang X 2013 Angew. Chem. In. Ed. 52 9719
 Google Scholar
Google Scholar
[53] Zhou F, Cui X, Shang A, Lian J, Yang L, Jin Y, Li B 2017 Microchim. Acta 184 773
 Google Scholar
Google Scholar
[54] Ai J, Guo W, Li B, Li T, Li D, Wang E 2012 Talanta 88 450
 Google Scholar
Google Scholar
[55] Fu Y, Zhao X, Zhang J, Li W 2014 J. Phys. Chem. C 118 18116
 Google Scholar
Google Scholar
[56] Li W, Li W, Hu Y, Xia Y, Shen Q, Nie Z, Huang Y, Yao S 2013 Biosen. Bioelectron. 47 345
 Google Scholar
Google Scholar
[57] Wu L L, Wang L Y, Xie Z J, Pan N, Peng C F 2016 Sens. Actuators, B 235 110
 Google Scholar
Google Scholar
[58] Navani N K, Li Y 2006 Curr. Opin. Chem. Biol. 10 272
 Google Scholar
Google Scholar
[59] Stoltenburg R, Reinemann C, Strehlitz B 2007 Biomol. Eng. 24 381
 Google Scholar
Google Scholar
[60] Zhan S, Wu Y, Wang L, Zhan X, Zhou P 2016 Biosens Bioelectron. 86 353
 Google Scholar
Google Scholar
[61] Dass C R, Choong P F, Khachigian L M 2008 Mol. Cancer Ther. 7 243
 Google Scholar
Google Scholar
[62] McGhee C E, Loh K Y, Lu Y 2017 Curr. Opin. Biotechnol. 45 191
 Google Scholar
Google Scholar
[63] Fan H, Zhang X, Lu Y 2017 Sci. China Chem. 60 591
 Google Scholar
Google Scholar
[64] Li L, Xu S, Yan H, Li X, Yazd H S, Li X, Huang T, Cui C, Jiang J, Tan W 2020 Angew. Chem. Int. Ed. 59 2
 Google Scholar
Google Scholar
[65] Pang X, Cui C, Wan S., Jiang Y, Zhang L, Xia L, Li L, Li X, Tan W 2018 Cancers 10 47
 Google Scholar
Google Scholar
[66] Meng H M, Liu H, Kuai H, Peng R, Mo L, Zhang X B 2016 Chem. Soc. Rev. 45 2583
 Google Scholar
Google Scholar
[67] Li S, Xu J, Wang S, Xia X, Chen L, Chen Z 2019 Chinese Chem. Lett. 30 1581
 Google Scholar
Google Scholar
[68] Zhang D, Yin L, Meng Z, Yu A, Guo L, Wang H 2014 Anal. Chim. Acta 812 161
 Google Scholar
Google Scholar
[69] Lei Y M, Huang W X, Zhao M, Chai Y Q, Yuan R, Zhuo Y 2015 Anal. Chem. 87 7787
[70] 陈俊俊, 李称, 徐斐, 曹慧, 叶泰, 于劲松, 袁敏 2018 工业微生物 3 11
 Google Scholar
Google Scholar
Chen J J, Li C, Xu F, Cao H, Ye T, Y u, J S, Yuan M 2018 Industrial Microorganisms 3 11
 Google Scholar
Google Scholar
[71] Williamson J R 1994 Annu. Rev. Bioph. Biom. 23 703
 Google Scholar
Google Scholar
[72] Chung C H, Kim J H, Jung J, Chung B H 2013 Biosen. Bioelectron. 41 827
 Google Scholar
Google Scholar
[73] Peng Y, Li Y, Li L, Zhu J J 2018 J. Hazard. Mater. 359 121
 Google Scholar
Google Scholar
[74] Breaker R R, Joyce G F 1994 Chem. Biol. 1 223
 Google Scholar
Google Scholar
[75] Ihms H E, Lu Y 2012 Humana Press 848 297
 Google Scholar
Google Scholar
[76] Liang W B, Zhuo Y, Zheng Y N, Xiong C Y, Chai Y Q, Yuan R 2017 ACS Appl. Mater. Interfaces 9 39812
 Google Scholar
Google Scholar
[77] Hong C, Kim D M, Baek A, Chung H, Jung W, Kim D E 2015 Chem. Commun. 51 5641
 Google Scholar
Google Scholar
[78] Chen J, Zuehlke A, Deng B, Peng H, Hou X, Zhang H 2017 Anal. Chem. 89 12888
 Google Scholar
Google Scholar
[79] Fan H, Zhao Z, Yan G, Zhang X, Yang C, Meng H, Chen Z, Liu H, Tan W 2015 Angew. Chem. 127 4883
 Google Scholar
Google Scholar
[80] Wang H, Wang H, Wu Q, Liang M, Liu X, Wang F 2019 Chem. Sci. 10 9597
 Google Scholar
Google Scholar
[81] Khakshoor O, Kool E T 2011 Chem. Commun. 47 7018
 Google Scholar
Google Scholar
[82] Pinheiro V B, Holliger P 2012 Curr. Opin. Chem. Biol. 16 245
 Google Scholar
Google Scholar
[83] Nielsen P E, Haaima G 1997 Chem. Soc. Rev. 26 73
 Google Scholar
Google Scholar
[84] Corradini R, Sforza S, Tedeschi T, Totsingan F, Manicardi A, Marchelli R 2011 Curr. Top. Med. Chem. 11 1535
 Google Scholar
Google Scholar
[85] Whittell G R, Manners I 2007 Adv. Mater. 19 3439
 Google Scholar
Google Scholar
[86] James H R 2012 Chem. Commun. 48 12165
 Google Scholar
Google Scholar
[87] Clever G H, Shionoya M 2010 Coord. Chem. Rev. 254 2391
 Google Scholar
Google Scholar
[88] Johannsen S, Megger N, Böhme D, Sige R K, Mn F, Manicard Nat. Chem. 2 229
[89] Zhu T, Wu Q, Chen P, Ding Y 2009 J. Organomet. Chem. 694 21
 Google Scholar
Google Scholar
[90] Li D, Song S, Fan C 2010 Accounts Chem. Res. 43 631
 Google Scholar
Google Scholar
[91] Abdullah R, Xie S, Wang R, Jin C, Du Y, Fu T, Li J, Zhang L, Tan W 2018 Anal. Chem. 91 2074
 Google Scholar
Google Scholar
[92] Wang R, Zhu G, Mei L, Xie Y, Ma H, Ye M, Qing F L, Tan W 2014 J. Am. Chem. Soc. 136 2731
 Google Scholar
Google Scholar
[93] Jin C, Liu X, Bai H, Wang R, Tan J, Peng X, Tan W 2017 ACS Nano 11 12087
 Google Scholar
Google Scholar
[94] Jin C, He J, Zou J, Xuan W, Fu T, Wang R, Tan W 2019 Nat. Commun. 10 2704
 Google Scholar
Google Scholar
[95] Xie S, Qiu L, Cui L, Liu H, Sun Y, Liang H, Ding D, He L, Liu H, Zhang J, Chen, Z. Zhang X, Tan W 2017 Chem 3 1021
 Google Scholar
Google Scholar
[96] Tan J, Li H, Hu X, Abdullah R, Xie S, Zhang L, Zhao M, Luo Q, Li Y, Sun Z, Yuan Q, Tan W 2019 Chem 5 1775
 Google Scholar
Google Scholar
[97] Zhang L, Abdullah R, H X, Bai H, Fan H, He L, Liang H, Zou J, Liu Y, Zhang, X. Tan W 2019 J. Am. Chem. Soc. 141 4282
 Google Scholar
Google Scholar
[98] Kallenbach N R, Ma R I, Seeman N C 1983 Nature 305 829
 Google Scholar
Google Scholar
[99] Seeman N C 2003 Nature 421 427
 Google Scholar
Google Scholar
[100] Aldaye F A, Palmer A L, Sleiman H F 2008 Science 321 1795
 Google Scholar
Google Scholar
[101] Seeman N C 2010 Annu. Rev. Biochem. 79 6
 Google Scholar
Google Scholar
[102] Wang Z G, Ding B 2014 Accounts Chem. Res. 47 1654
 Google Scholar
Google Scholar
[103] Veneziano R, Moyer T J, Stone M B, Wamhoff E C, Read B J, Mukherjee S, Shepherd T R, Das J, Schief W R, Irvine D J, Bathe M 2020 Nat. Nanotechnol. 15 716
 Google Scholar
Google Scholar
[104] He X, Dong L, Wang W, Lin N, Mi Y 2013 Chem. Commun. 49 2906
 Google Scholar
Google Scholar
[105] Liu Y, Chen Q, Liu J, Yang X, Guo Q, Li L, Liu W, Wang K 2017 Anal. Chem. 89 3590
 Google Scholar
Google Scholar
[106] Ke Y, Sharma J, Liu M, Jahn K, Liu Y, Yan H 2009 Nano Lett. 9 2445
 Google Scholar
Google Scholar
[107] Sadowski J P, Calvert C R, Zhang D Y, Pierce N A, Yin P 2014 ACS Nano 8 3251
 Google Scholar
Google Scholar
[108] Mou Q, Ma Y, Pan G, Xue B, Yan D, Zhang C, Zhu X 2017 Angew. Chem. 129 12702
 Google Scholar
Google Scholar
[109] Shiu S C C, Fraser L A, Ding Y, Tanner J A 2018 Molecules 23 1695
 Google Scholar
Google Scholar
[110] Um S H, Lee J B, Park N, Kwon, S Y, Umbach C C, Luo D 2006 Nat. Mater. 5 797
 Google Scholar
Google Scholar
[111] Shahbazi M A, Baulethk N, Kwon, S Y, Umbach C C Adv. Therap. 1 1800042
[112] He Y, Tian Y, Chen Y, Deng Z, Ribbe A E, Mao C 2005 Angew. Chem. Int. Ed. 44 6694
 Google Scholar
Google Scholar
[113] He Y, Chen Y, Liu H, Ribbe A E, Mao C 2005 J. Am. Chem. Soc. 127 12202
 Google Scholar
Google Scholar
[114] Douglas S M, Marblestone A H, Teerapittayanon S, Vazquez A, Church G M, Shih W M 2009 Nucleic Acids Res. 37 5001
 Google Scholar
Google Scholar
[115] Bila H, Kurisinkal E E, Bastings M M 2019 Biomater. Sci. 7 532
 Google Scholar
Google Scholar
[116] Rothemund P W K 2006 Nature 440 297
 Google Scholar
Google Scholar
[117] Veneziano R, Ratanalert S, Zhang K, Zhang F, Yan H, Chiu W, Bathe M 2016 Science 352 1534
 Google Scholar
Google Scholar
[118] Schreiber R, Do J, Roller E M, Zhang T, Sch, ler, V J, Nickels P C, Feldmann J, Liedl T 2014 Nat. Nanotechnol. 9 74
 Google Scholar
Google Scholar
[119] Zhan P, Wen T, Wang Z G, He Y, Shi J, Wang T. Liu X, Lu G, Ding B 2018 Angew. Chem. Int. Ed. 57 2846
 Google Scholar
Google Scholar
[120] Ding B, Deng Z, Yan H, Cabrini S, Zuckermann R N, Bokor J 2010 J. Am. Chem. Soc. 132 3248
 Google Scholar
Google Scholar
[121] Tian Y, Wang T, Liu W, Xin H L, Li H, Ke Y, M. Shih W, Gang O 2015 Nat. Nanotechnol. 10 637
 Google Scholar
Google Scholar
[122] Jia S, Wang J, Xie M, Sun J, Liu H, Zhang Y, Chao J, Li J, Wang L, Lin J, Gothelf K V, Fan C 2019 Nat. Commun. 10 5597
 Google Scholar
Google Scholar
[123] Liu X, Zhang F, Jing X, Pan M, Liu P, Li W, Zhu B, Li J, Chen H, Wang L, Lin J, Liu Y, Zhao D, Yan H, Fan C 2018 Nature 559 593
 Google Scholar
Google Scholar
[124] Schreiber R, Luong N, Fan, Z, Kuzyk A, Nickels P C, Zhang T, Smith D M, Yurke B, Kuang W, Govorov A O, Liedl T 2013 Nat. Commun. 4 1
 Google Scholar
Google Scholar
[125] Urban M J, Dutta P K, Wang P, Duan, X, Shen X, Ding B, Ke Y, Liu N 2016 J. Am. Chem. Soc. 138 5495
 Google Scholar
Google Scholar
[126] Wang P, Meyer T A, Pan V, Dutta P K, Ke Y 2017 Chem 2 359
 Google Scholar
Google Scholar
[127] Loretan M, Domljanovic I, Lakatos M, Re Y 2017 Ding B, Ke Y Materials 13 2185
 Google Scholar
Google Scholar
[128] Fu J, Liu M, Liu Y, Woodbury N W, Yan H 2012 J. Am. Chem. Soc. 134 5516
 Google Scholar
Google Scholar
[129] Liu N, Dai M, Saka S K, Yin P 2019 Nat. Chem. 11 1001
 Google Scholar
Google Scholar
[130] Braun E, Eichen Y, Sivan U, Ben-Yoseph G 1998 Nature 391 775
 Google Scholar
Google Scholar
[131] Liu J, Geng Y, Pound E, Gyawali S, Ashton J R, Hickey J, Woolley A T, Harb J N 2011 ACS Nano 5 2240
 Google Scholar
Google Scholar
[132] Geng Y, Liu J, Pound E, Gyawali S, Harb J N, Woolley A T 2011 J. Mater. Chem. 21 12126
 Google Scholar
Google Scholar
[133] Geng Y, Pearson A C, Gates E P, Uprety B, Davis R C, Harb J N, Woolley A T 2013 Langmuir 29 3482
 Google Scholar
Google Scholar
[134] Pilo-Pais M, Goldberg S, Samano E, LaBean T H, Finkelstein G 2011 Nano Lett. 11 3489
 Google Scholar
Google Scholar
[135] Helmi S, Ziegler C, Kauert D J, Seidel R 2014 Nano Lett. 14 6693
 Google Scholar
Google Scholar
[136] Sun W, Boulais E, Hakobyan Y, Wang W L, Guan A, Bathe M, Yin P 2014 Science 346 6210
 Google Scholar
Google Scholar
计量
- 文章访问数: 19475
- PDF下载量: 307
- 被引次数: 0












 下载:
下载: