-
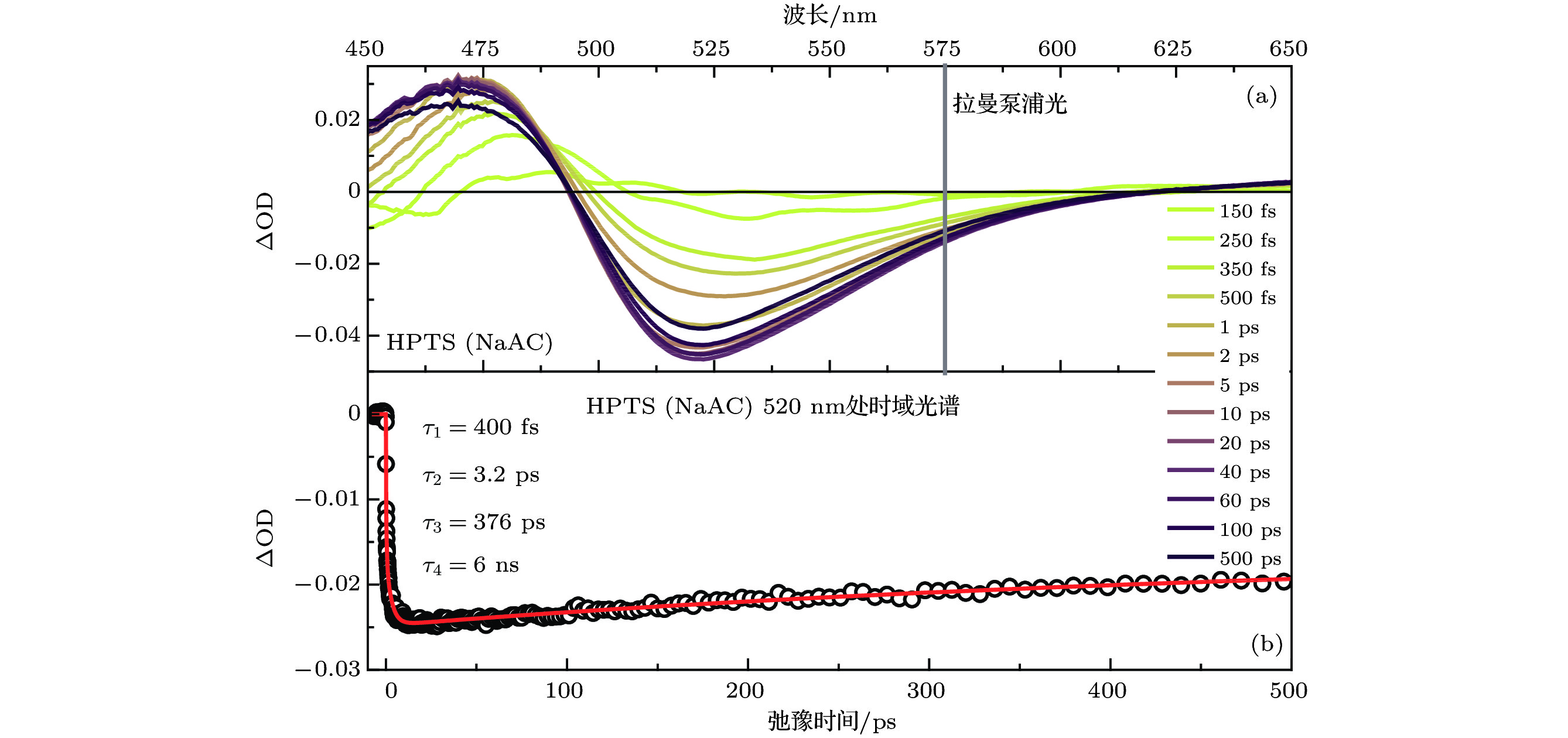
As one of the most fundamental processes, proton transfer reaction plays an important role in chemical and biological process, and to reveal the choreography of the proton motion intra- and intermolecularly, a spectroscopic technique capable of capturing molecular structural dynamics of excited-state proton transfer motions on an intrinsic time scale is needed. In this study, We utilize wavelength-tunable femtosecond stimulated Raman spectroscopy with a time resolution of ~100 fs, spectral resolution of 15 cm–1 and spectral range of 400 cm–1—1800 cm–1, combined with traditional transient absorption spectroscopywith a time window between 0 and 600 ps to simultaneously achieve reaction dynamics for transient reactant and product of the photoacid pyranine (8-hydroxypyrene1, 3, 6-trisulfonic acid, HPTS) molecules undergoing excited-state proton transfer reaction in complex with water and acetate molecules. Marker bands attributed to the deprotonated form of HPTS in a frequency range from 400 cm–1 to 1700 cm–1 are obtained under the excitation of 400 nm laser pulses. The marker band at 1516 cm–1, which is assigned to phenolic ring carbon carbon double band stretching accompanied with carbon hydrogen in-plane rocking motions, exhibits complex rise and decay dynamics. The simultaneously observed excited-state Raman mode at 920 cm–1 which is assigned to the excited carbon-carbon single bond stretch mode in the protonated acetic acid root molecule, helps us to clearly resolve the reaction rates of excited-state proton transfer. Based on the multi-exponential fitting results, the dynamics of excited-state Raman mode at 920 cm–1 exhibits bi-exponential processes with time constants of ~470 fs and ~3 ps. The ultrafast time component indicates that the excited-state proton transfer originates from an HPTS-acetate complex, indicating that part of the ground-state HPTS molecules are in the “tight” hydrogen bonding configuration that can quickly shift the excited-state proton charge toward the acetate acceptor molecule through a direct hydrogen bond. The second slower time component implies a significant subpopulation of HPTS in the ground state, i.e. hydrogen bonds to an acetate ion via an intervening water molecule, and upon photo excitation, the proton transfers to the water solvent before proton is picked up by the acetate ion.
-
Keywords:
- femtosecond stimulated Raman spectroscopy /
- transient absorption spectrum /
- excited state proton transfer /
- photoacid
[1] Weinberg D R, Gagliardi C J, Hull J F, MurpHy C F, Kent C A, Westlake B C, Paul A, Ess D H, McCafferty D G, Meyer T J 2012 Chem. Rev. 112 4016
 Google Scholar
Google Scholar
[2] Hayashi S, Tajkhorshid E, Schulten K 2002 Biophys. J. 83 1281
 Google Scholar
Google Scholar
[3] Jacquemin D, Zuniga J, Requena A, Céron-Carrasco J P 2014 Accounts Chem. Res. 47 2467
 Google Scholar
Google Scholar
[4] Fang C, Frontiera R R, Tran R, Mathies R A 2009 Nature 462 200
 Google Scholar
Google Scholar
[5] Oscar B G, Liu W, Zhao Y, Tang L, Wang Y, Campbell R E, Fang C 2014 Proc. Natl. Acad. Sci. U.S.A. 111 10191
 Google Scholar
Google Scholar
[6] Chou P, McMorrow D, Aartsma T, Kasha M 1984 J. Phys. Chem. 88 4596
 Google Scholar
Google Scholar
[7] Zhao J, Ji S, Chen Y, Guo H, Yang P 2012 Phys. Chem. Chem. Phys. 14 8803
 Google Scholar
Google Scholar
[8] Tseng H W, Liu J Q, Chen Y A, Chao C M, Liu K M, Chen C L, Lin T C, Hung C H, Chou Y L, Lin T C 2015 Chem. Phys. Lett. 6 1477
 Google Scholar
Google Scholar
[9] Kwon J E, Park S Y 2011 Adv. Mater. 23 3615
 Google Scholar
Google Scholar
[10] Chudoba C, Riedle E, Pfeiffer M, Elsaesser T 1996 Chem. Phys. lett. 263 622
 Google Scholar
Google Scholar
[11] Leiderman P, Genosar L, Huppert D 2005 J. Phys. Chem. A 109 5965
 Google Scholar
Google Scholar
[12] Tran-Thi T H, Gustavsson T, Prayer C, Pommeret S, Hynes J T 2000 Chem. Phys. Lett. 329 421
 Google Scholar
Google Scholar
[13] Kukura P, Frontiera R, Mathies R A 2006 Phys. Rev. Lett. 96 238303
 Google Scholar
Google Scholar
[14] Frontiera R, Mathies R A 2011 Laser Photonics Rev. 5 102
 Google Scholar
Google Scholar
[15] 赵晓辉, 马菲, 吴义室, 艾希成, 张建平 2008 物理学报 57 298
 Google Scholar
Google Scholar
Zhao X H, Ma F, Wu Y S, Ai X C 2008 Acta Phys. Sin. 57 298
 Google Scholar
Google Scholar
[16] Chen C, Zhu L D, Boulanger S A, Baleeva N S, Myasnyanko I N, Baranov M S, Fang C 2020 J. Chem. Phys. 152 021101
 Google Scholar
Google Scholar
[17] Fang C, Tang L T, Oscar B G, Chen C 2018 J. Phys. Chem. Lett. 9 3253
 Google Scholar
Google Scholar
[18] Liu W M, Han F Y, Smith C, Fang C 2012 J. Phys. Chem. B 116 10535
 Google Scholar
Google Scholar
[19] Han F Y, Liu W M, Fang C 2013 Chem. Phys. 422 204
 Google Scholar
Google Scholar
[20] Wang Y L, Liu W M, Tang L T, Oscar B, Han F, Fang C 2013 J. Phys. Chem. A 117 6024
 Google Scholar
Google Scholar
[21] Liu W M, Wang Y L, Tang L T, Oscar B G, Zhu L D, Fang C 2016 Chem. Sci. 7 5484
 Google Scholar
Google Scholar
[22] Liu W M, Tang L T, Oscar B G, Wang Y L, Chen C, Fang C 2017 J. Phys. Chem. Lett. 8 997
 Google Scholar
Google Scholar
[23] Oscar B G, Chen C, Liu W M, Zhu L D, Fang C 2017 J. Phys. Chem. A 121 5428
 Google Scholar
Google Scholar
[24] Tang L T, Wang Y L, Zhu L D, Lee C, Fang C 2018 J. Phys. Chem. Lett. 9 2311
 Google Scholar
Google Scholar
[25] Chakraborty S, Nandi S, Bhattacharyya K, Mukherjee S 2019 ChemPhysChem 20 3221
 Google Scholar
Google Scholar
[26] Siwick B J, Bakker H J 2007 J. Am. Chem. Soc. 129 13412
 Google Scholar
Google Scholar
-
图 2 (a) HPTS分子从质子化状态(左)经光激发转变为去质子化状态(右); (b) HPTS分别在NaAC溶液(蓝色), pH = 12水溶液(绿色)和pH = 4.5水溶液(黑色)中的稳态吸收光谱(实线)以及荧光发射光谱(虚线)
Fig. 2. (a) The molecular structure of HPTS in one simple H-bonding geometry with acetate ion; (b) the steady-state absorption (solid line) and fluorescence emission spectra (dash dot line) of HPTS in aqueous solution (pH = 4.5, black; pH = 12, green) and acetate solution (blue).
图 5 (a) HPTS(NaAC)和(b) HPTS(pH = 12)在1615 cm–1的FSRS动力学光谱; (c) HPTS(NaAC)在920 cm–1的FSRS动力学光谱; (d) HPTS(NaAC)和HPTS(pH=12)在1615 cm–1处时间窗口为1.5 ps的FSRS动力学光谱; (e) HPTS去质子状态下1615 cm–1的拉曼振动模式示意图
Fig. 5. Excited-state Raman dynamics spectra of (a) HPTS (NaAC) at 1615 cm–1 and (b) HPTS (pH = 12) at 1615 cm–1; (c) excited-state Raman dynamics spectra of HPTS (NaAC) at 920 cm–1; (d) excited-state Raman dynamics spectra of HPTS (NaAC) and HPTS (pH = 12) at 1615 cm–1 present in the time window of 1.5 ps; (e) Raman vibrational motions of deprotonated HPTS at 1615 cm–1.
-
[1] Weinberg D R, Gagliardi C J, Hull J F, MurpHy C F, Kent C A, Westlake B C, Paul A, Ess D H, McCafferty D G, Meyer T J 2012 Chem. Rev. 112 4016
 Google Scholar
Google Scholar
[2] Hayashi S, Tajkhorshid E, Schulten K 2002 Biophys. J. 83 1281
 Google Scholar
Google Scholar
[3] Jacquemin D, Zuniga J, Requena A, Céron-Carrasco J P 2014 Accounts Chem. Res. 47 2467
 Google Scholar
Google Scholar
[4] Fang C, Frontiera R R, Tran R, Mathies R A 2009 Nature 462 200
 Google Scholar
Google Scholar
[5] Oscar B G, Liu W, Zhao Y, Tang L, Wang Y, Campbell R E, Fang C 2014 Proc. Natl. Acad. Sci. U.S.A. 111 10191
 Google Scholar
Google Scholar
[6] Chou P, McMorrow D, Aartsma T, Kasha M 1984 J. Phys. Chem. 88 4596
 Google Scholar
Google Scholar
[7] Zhao J, Ji S, Chen Y, Guo H, Yang P 2012 Phys. Chem. Chem. Phys. 14 8803
 Google Scholar
Google Scholar
[8] Tseng H W, Liu J Q, Chen Y A, Chao C M, Liu K M, Chen C L, Lin T C, Hung C H, Chou Y L, Lin T C 2015 Chem. Phys. Lett. 6 1477
 Google Scholar
Google Scholar
[9] Kwon J E, Park S Y 2011 Adv. Mater. 23 3615
 Google Scholar
Google Scholar
[10] Chudoba C, Riedle E, Pfeiffer M, Elsaesser T 1996 Chem. Phys. lett. 263 622
 Google Scholar
Google Scholar
[11] Leiderman P, Genosar L, Huppert D 2005 J. Phys. Chem. A 109 5965
 Google Scholar
Google Scholar
[12] Tran-Thi T H, Gustavsson T, Prayer C, Pommeret S, Hynes J T 2000 Chem. Phys. Lett. 329 421
 Google Scholar
Google Scholar
[13] Kukura P, Frontiera R, Mathies R A 2006 Phys. Rev. Lett. 96 238303
 Google Scholar
Google Scholar
[14] Frontiera R, Mathies R A 2011 Laser Photonics Rev. 5 102
 Google Scholar
Google Scholar
[15] 赵晓辉, 马菲, 吴义室, 艾希成, 张建平 2008 物理学报 57 298
 Google Scholar
Google Scholar
Zhao X H, Ma F, Wu Y S, Ai X C 2008 Acta Phys. Sin. 57 298
 Google Scholar
Google Scholar
[16] Chen C, Zhu L D, Boulanger S A, Baleeva N S, Myasnyanko I N, Baranov M S, Fang C 2020 J. Chem. Phys. 152 021101
 Google Scholar
Google Scholar
[17] Fang C, Tang L T, Oscar B G, Chen C 2018 J. Phys. Chem. Lett. 9 3253
 Google Scholar
Google Scholar
[18] Liu W M, Han F Y, Smith C, Fang C 2012 J. Phys. Chem. B 116 10535
 Google Scholar
Google Scholar
[19] Han F Y, Liu W M, Fang C 2013 Chem. Phys. 422 204
 Google Scholar
Google Scholar
[20] Wang Y L, Liu W M, Tang L T, Oscar B, Han F, Fang C 2013 J. Phys. Chem. A 117 6024
 Google Scholar
Google Scholar
[21] Liu W M, Wang Y L, Tang L T, Oscar B G, Zhu L D, Fang C 2016 Chem. Sci. 7 5484
 Google Scholar
Google Scholar
[22] Liu W M, Tang L T, Oscar B G, Wang Y L, Chen C, Fang C 2017 J. Phys. Chem. Lett. 8 997
 Google Scholar
Google Scholar
[23] Oscar B G, Chen C, Liu W M, Zhu L D, Fang C 2017 J. Phys. Chem. A 121 5428
 Google Scholar
Google Scholar
[24] Tang L T, Wang Y L, Zhu L D, Lee C, Fang C 2018 J. Phys. Chem. Lett. 9 2311
 Google Scholar
Google Scholar
[25] Chakraborty S, Nandi S, Bhattacharyya K, Mukherjee S 2019 ChemPhysChem 20 3221
 Google Scholar
Google Scholar
[26] Siwick B J, Bakker H J 2007 J. Am. Chem. Soc. 129 13412
 Google Scholar
Google Scholar
计量
- 文章访问数: 12097
- PDF下载量: 190
- 被引次数: 0












 下载:
下载: