-
数字全息显微成像有别于传统光学显微成像, 可根据重建全息图获取细胞的生物学参数与形貌信息, 是一种有效的非接触无损三维成像技术. 随着像感器的发展与硬件计算能力的提升, 数字全息显微成像技术在活体生物细胞检测尤其在血红细胞检测领域取得了显著进展和突破. 本文介绍了同轴、离轴以及光镊辅助离轴的数字全息显微技术, 这些技术利用瑞利索末菲反向传播算法、清晰度量化算法、分水岭分割算法、数字重聚焦方法与热涨落方法等来实现血红细胞的形变、空间分布、三维体积信息的高精度提取, 有助于糖尿病、心血管疾病、帕金森氏疾病等病理研究. 数字全息显微成像技术实现了传统三维显微成像技术难以达到的实时性和定量化检测, 由于独有的非接触、无损性特点, 在细胞成像领域应用前景广阔.Digital holographic microscopy (DHM) can obtain biological parameters and morphological information of cells by reconstructing holograms, which is different from traditional optical microscopy. The DHM is a three-dimensional imaging technology which is effective, non-contact and non-destructive. With the developments of the image sensor and the computing technology, it has made significant progress in the field of living cells detection, especially for red blood cell. Compared with the technologies which are widely used in the field of cell imaging such as con-focal laser scanning microscopy, scanning near-field optical microscopy and optical coherence tomography, the DHM has the advantages including wide FOV and high-resolution to achieve higher imaging and quality. This paper introduces the principle of recording and reconstruction of digital holography, and then analyzes the performance of three reconstruction algorithms using the Fresnel method, the convolution method and the angular spectrum method. The Fresnel method is suitable for the sample size larger than the image sensor. Both the convolution method and the angular spectrum method have an optimal reconstruction distance. When the reconstruction distance is different from the optimal distance, the resolution of the reconstructed image will decrease, and the angular spectrum method is better than the convolution method in overall performance. The DHM system for RBC measurements mainly adopts the convolution algorithm or the angular spectrum algorithm to implement numerical reconstruction. The systems of the in-line DHM, the off-axis DHM and the optical tweezers combining with off-axis DHM are introduced. These techniques use algorithms including Rayleigh-Sommerfeld back-propagation, the sharpness quantification, the watershed segmentation, the numerical refocusing and the thermal fluctuation to determine the focal plane position and obtain the best reconstruction distance of the RBCs, and further detect the shape change of the RBCs and extract the information of high-resolution blood vessel shape and blood flow velocity. These techniques can even achieve the dynamic tracking and measure three-dimensional volume of RBCs in real-time which is helpful for pathological studies such as diabetes, cardiovascular disease and Parkinson's disease. With its unique non-contact and non-destructive characteristics, the DHM realizes real-time and quantitative detection that is difficult to achieve with traditional three-dimensional microscopic imaging technologies.
-
Keywords:
- digital holography /
- microscope /
- cell imaging /
- digital refocusing
[1] Cuche E, Marquet P, Depeursinge C 1999 Appl. Opt. 38 6994
 Google Scholar
Google Scholar
[2] Ferraro P, Coppola G, De Nicola S, Finizio A, Pierattini G 2003 Opt. Lett. 28 1257
 Google Scholar
Google Scholar
[3] Ferraro P, Miccio L, Grilli S, Paturzo M, De Nicola S, Finizio A, Osellame R, Laporta P 2007 Opt. Express 15 14591
 Google Scholar
Google Scholar
[4] Charrière F, Marian A, Montfort F, Kuehn J, Colomb T, Cuche E, Marquet P, Depeursinge C 2006 Opt. Lett. 31 178
 Google Scholar
Google Scholar
[5] Kemper B, Von Bally G 2008 Appl. Opt. 47 A52
 Google Scholar
Google Scholar
[6] Potcoava M, Kim M 2008 Meas Sci Technol 19 074010
 Google Scholar
Google Scholar
[7] 袁操今, 翟宏琛 2010 光子学报 39 893
 Google Scholar
Google Scholar
Yuan C J, Zhai H C 2010 Acta Phot. Sin. 39 893
 Google Scholar
Google Scholar
[8] Ma J, Yuan C, Situ G, Pedrini G, Osten W 2013 Chin. Opt. Lett. 11 090901
 Google Scholar
Google Scholar
[9] 王华英, 刘飞飞, 成惠, 廖薇, 赵宝群, 于梦杰, 刘佐强 2013 强激光与粒子束 25 345
 Google Scholar
Google Scholar
Wang H Y, Liu F F, Cheng H, Liao W, Zhao B Q, Yu M J, Liu Z Q 2013 High Pow Las Part Beam 25 345
 Google Scholar
Google Scholar
[10] 王华英, 刘飞飞, 宋修法, 廖微, 赵宝群, 于梦杰, 刘佐强 2013 物理学报 62 024207
 Google Scholar
Google Scholar
Wang H Y, Liu F F, Liao W, Song X F, Yu M J, Liu Z Q 2013 Acta Phys. Sin. 62 024207
 Google Scholar
Google Scholar
[11] Zheng J, Pedrini G, Gao P, Yao B, Osten W 2015 J. Opt. 17 085301
 Google Scholar
Google Scholar
[12] Lin Q, Wang D, Wang Y, Rong L, Chang S 2015 Opt. Lasers Eng. 66 279
 Google Scholar
Google Scholar
[13] Wang Y, Guo S, Wang D, Lin Q, Rong L, Zhao J 2016 Opt. Commun. 366 81
 Google Scholar
Google Scholar
[14] 董可平, 钱晓凡, 张磊, 张永安 2007 光子学报 36 2013
Dong K P, Qian X F, Zhang L, Zhang Y A 2007 Acta Phot. Sin. 36 2013
[15] 邸江磊, 赵建林, 范琦, 姜宏振, 孙伟伟 2008 光学学报 28 56
 Google Scholar
Google Scholar
Di J L, Zhao J L, Fan Q, Jiang H Z, Sun W W 2008 Acta Optic. Sin. 28 56
 Google Scholar
Google Scholar
[16] 马利红, 王辉, 金洪震, 李勇 2012 中国激光 39 215
Ma L H, Wang H, Jin H Z, Li Y 2012 Chin. J. Las. 39 215
[17] Cao R, Xiao W, Wu X, Sun L, Pan F 2018 Biomed. Opt. Express 9 72
 Google Scholar
Google Scholar
[18] Zhang J, Chen Q, Sun J, Zuo C 2019 Seventh International Conference on Optical and Photonic Engineering (icOPEN 2019), Phuket, Thailand, October 16, 2019 p112050 C
[19] Zhang J, Sun J, Chen Q, Zuo C 2020 IEEE Trans. Comput. Imaging. 6 697
 Google Scholar
Google Scholar
[20] Amos W, White J 2003 Biol. Cell 95 335
 Google Scholar
Google Scholar
[21] Subramaniam V, Kirsch A, Jovin T 1998 Cell. Mol. Biol. (Noisy-le-grand) 44 689
[22] Huang D, Swanson E A, Lin C P, Schuman J S, Stinson W G, Chang W, Hee M R, Flotte T, Gregory K, Puliafito C A 1991 Science 254 1178
 Google Scholar
Google Scholar
[23] Kemper B, Carl D, Knoche S, Thien R, von Bally G 2004 Optical Metrology in Production Engineering Strasbourg, France, September 10, 2004 p581
[24] Jin H, Wan H, Zhang Y, Li Y, Qiu P 2008 J. Mod. Opt. 55 2989
 Google Scholar
Google Scholar
[25] 周海宪 2006 应用光学 27 I0007
Zhou H X 2006 J. Appl. Opt. 27 I0007
[26] Nehmetallah G T, Aylo R, Williams L 2015 Analog and Digital Holography with MATLAB (Bellingham: Society of Photo-Optical Instrumentation Engineers (SPIE)) pp137–143
[27] Kreis T M, Adams M, Jüptner W P 1997 Optical Inspection and Micromeasurements II Munich, Germany, September 17, 1997 p224
[28] Liu C, Wang D, Zhang Y 2009 Opt. Eng. 48 105802
 Google Scholar
Google Scholar
[29] Song X, Zhao B, Qin A 4th International Symposium on Advanced Optical Manufacturing Chengdu, China, November 19−21, 2008 p728340
[30] Huaying W, Baoqun Z, Wei L 2009 IEEE International Conference on Intelligent Computing and Intelligent Systems, Shanghai, China, November 20−22, 2009 p838
[31] 王广俊, 王大勇, 王华英 2010 激光与光电子学进展 47 030901
 Google Scholar
Google Scholar
Wang G J, Wang D Y, Wang H Y 2010 Laser Optoelectron. Prog. 47 030901
 Google Scholar
Google Scholar
[32] Goodman J W 2005 Introduction To Fourier Optics (Placerville: Roberts and Company Publishers) pp298–306
[33] Lai S, King B, Neifeld M A 2000 Opt. Commun. 173 155
 Google Scholar
Google Scholar
[34] Yamaguchi I, Zhang T 1997 Opt. Lett. 22 1268
 Google Scholar
Google Scholar
[35] Kim M-K 2010 J. Opt. Soc. Korea 14 77
 Google Scholar
Google Scholar
[36] Colomb T, Cuche E, Charrière F, Kühn J, Aspert N, Montfort F, Marquet P, Depeursinge C 2006 Appl. Opt. 45 851
 Google Scholar
Google Scholar
[37] 惠梅, 王东生, 李庆祥, 邓年茂, 徐毓娴 2003 光学学报 23 1245
 Google Scholar
Google Scholar
Hui M, Wang D S, Li Q X, Deng N M, Xu Y X 2003 Acta Optic. Sin. 23 1245
 Google Scholar
Google Scholar
[38] 葛宝臻, 崔鹏, 吕且妮, 魏耀林 2008 中国石油大学学报: 自然科学版 32 169
Ge B Z, Cui P, Lv Q N, Wei Y L 2008 J. China U. Pet.: Nat. Sci. Ed. 32 169
[39] 朱娜娜, 金孝岠, 郭建荣 2019 中国糖尿病杂志 27 12
Zhu N N, Jin X J, Guo J R 2019 Chin. J. Diabetes Mellitus 27 12
[40] Lee S, Park H, Kim K, Sohn Y, Jang S, Park Y 2017 Sci. Rep. 7 1
 Google Scholar
Google Scholar
[41] 丁宁, 陈长强, 樊绮诗 2019 检验医学 34 889
Ding N, Chen C Q, Fan Q S 2019 Lab. Med. 34 889
[42] Li N, Zhou H, Tang Q 2017 Dis. Markers 2017 1
[43] Jenner P 2003 Ann. Neurol. 53 S26
 Google Scholar
Google Scholar
[44] Hald A, Lotharius J 2005 Exp. Neurol. 193 279
 Google Scholar
Google Scholar
[45] Spirito P, Maron B J, Bonow R O 1986 J. Am. Coll. Cardiol. 7 518
 Google Scholar
Google Scholar
[46] Harders A G, Gilsbach J M 1987 J. Neurosurg. 66 718
 Google Scholar
Google Scholar
[47] Sugii Y, Okuda R, Okamoto K, Madarame H 2005 Meas. Sci. Technol. 16 1126
 Google Scholar
Google Scholar
[48] Lima R, Wada S, Takeda M, Tsubota K-i, Yamaguchi T 2007 J. Biomech. 40 2752
 Google Scholar
Google Scholar
[49] Jia Y, Morrison J C, Tokayer J, Tan O, Lombardi L, Baumann B, Lu C D, Choi W, Fujimoto J G, Huang D 2012 Biomed. Opt. Express 3 3127
 Google Scholar
Google Scholar
[50] van den Berg P, Daoudi K, Steenbergen W 2015 Photoacoustics 3 89
 Google Scholar
Google Scholar
[51] Choi Y S, Lee S J 2009 Appl. Opt. 48 2983
 Google Scholar
Google Scholar
[52] Zakrisson J, Schedin S, Andersson M 2015 Appl. Opt. 54 7442
 Google Scholar
Google Scholar
[53] Rinehart M T, Park H S, Wax A 2015 Biomed. Opt. Express 6 2067
 Google Scholar
Google Scholar
[54] Yi F, Lee C-G, Moon I-K 2012 J. Opt. Soc. Korea 16 115
 Google Scholar
Google Scholar
[55] Fällman E, Schedin S, Jass J, Andersson M, Uhlin B E, Axner O 2004 Biosens. Bioelectron. 19 1429
 Google Scholar
Google Scholar
[56] Andersson M, Fällman E, Uhlin B E, Axner O 2006 Biophys. J. 91 2717
 Google Scholar
Google Scholar
[57] Groen F C, Young I T, Ligthart G 1985 Cytometry A 6 81
 Google Scholar
Google Scholar
[58] Sheng J, Malkiel E, Katz J 2006 Appl. Opt. 45 3893
 Google Scholar
Google Scholar
[59] Langehanenberg P, Kemper B, Dirksen D, Von Bally G 2008 Appl. Opt. 47 D176
 Google Scholar
Google Scholar
[60] Moon I, Daneshpanah M, Javidi B, Stern A 2009 Proc. IEEE Inst. Electr. Electron Eng. 97 990
 Google Scholar
Google Scholar
[61] Moon I, Javidi B, Yi F, Boss D, Marquet P 2012 Opt. Express 20 10295
 Google Scholar
Google Scholar
[62] Gonzalez R, Woods R E 2002 Digital Image Processing (New York: Prentice-Hall) pp588−596
[63] Rencher A C 1998 Multivariate Statistical Inference and Applications (New York: Wiley) pp41−63
[64] Masters B R 2012 J. Biomed. Opt. 17 029901
 Google Scholar
Google Scholar
[65] Mir M, Wang Z, Shen Z, Bednarz M, Bashir R, Golding I, Prasanth S G, Popescu G 2011 P NATL ACAD SCI USA 108 13124
 Google Scholar
Google Scholar
[66] Shaked N T, Finan J D, Guilak F, Wax A P 2010 J Biomed Opt 15 010505
 Google Scholar
Google Scholar
[67] Park Y, Diez-Silva M, Popescu G, Lykotrafitis G, Choi W, Feld M S, Suresh S 2008 Proc. Natl. Acad. Sci. 105 13730
 Google Scholar
Google Scholar
[68] Dubois F, Schockaert C, Callens N, Yourassowsky C 2006 Opt. Express 14 5895
 Google Scholar
Google Scholar
[69] Xu L, Mater M, Ni J 2011 Opt. Express 19 14779
 Google Scholar
Google Scholar
[70] Liebling M, Unser M 2004 J. Opt. Soc. Am. A. Opt. Image. Sci. Vis. 21 2424
 Google Scholar
Google Scholar
[71] Hwang O 2013 Exp. Neurobiol. 22 11
 Google Scholar
Google Scholar
[72] Liu J, Zhu L, Zhang F, Dong M, Qu X 2019 Appl. Opt. 58 4042
 Google Scholar
Google Scholar
[73] Felgner H, Müller O, Schliwa M 1995 Appl. Opt. 34 977
 Google Scholar
Google Scholar
[74] Florin E-L, Pralle A, Stelzer E, Hörber J 1998 Appl. Phys. A 66 S75
 Google Scholar
Google Scholar
[75] Schlenker T, Feranchak A P, Schwake L, Stremmel W, Roman R M, Fitz J G 2000 Gastroenterology 118 395
 Google Scholar
Google Scholar
-
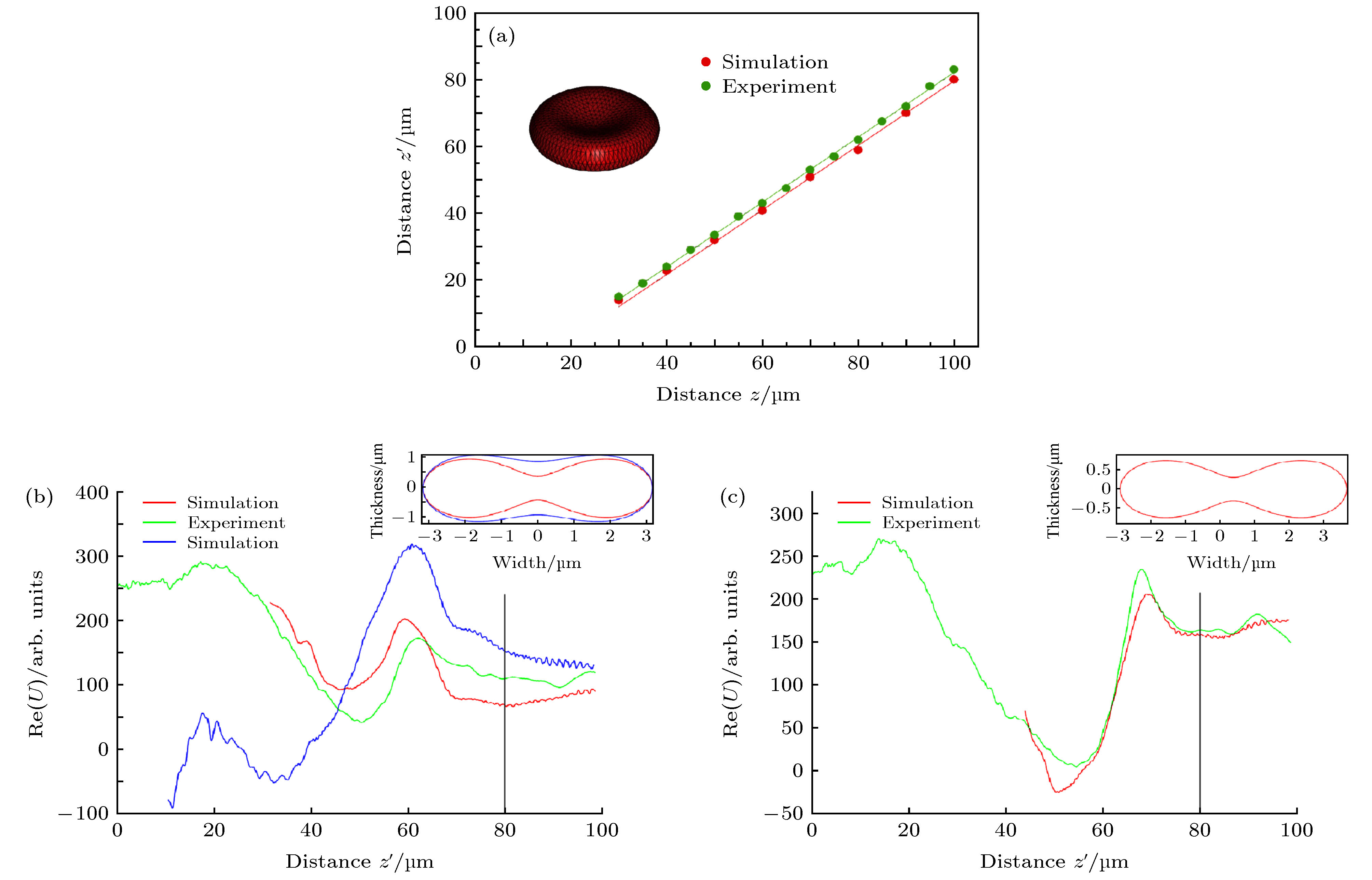
图 4 RBC形变与重建的复振幅实部信息之间联系的结果分析 (a)不同记录距离z下最佳反向重建距离z', 绿线代表实际实验, 红线代表模拟实验, 插图代表模拟实验所用RBC; (b)绿线代表实际实验RBC的Re(U), 红线与紫线分别代表模拟实验中初始RBC与变形后RBC的Re(U); (c)所用RBC比(b)所用小约20%, 绿线与红线分别代表实际实验与模拟实验所得Re(U)结果; (b)与(c)所用黑线表示RBC的记录距离[52]
Fig. 4. The relationship between the RBC deformation and the real part of reconstructed amplitude. (a) The reconstruction distance z' to the focus at different recording distances z of the simulated RBC (red) and the experiment using a real RBC (green). Inset shows the Cassini model of the RBC used in the simulations; (b) the experiment using a real RBC (green), the reconstructed Re(U) for the simulated unaltered RBC and a deformed RBC represented by the red and blue curves, respectively; (c) reconstructed data from a ~20% smaller RBC compared with the one used in (b). Red and green curves represent the Re(U) of simulation and experiment, respectively; Gray vertical line in (b) and (c) indicates position of the RBC[52].
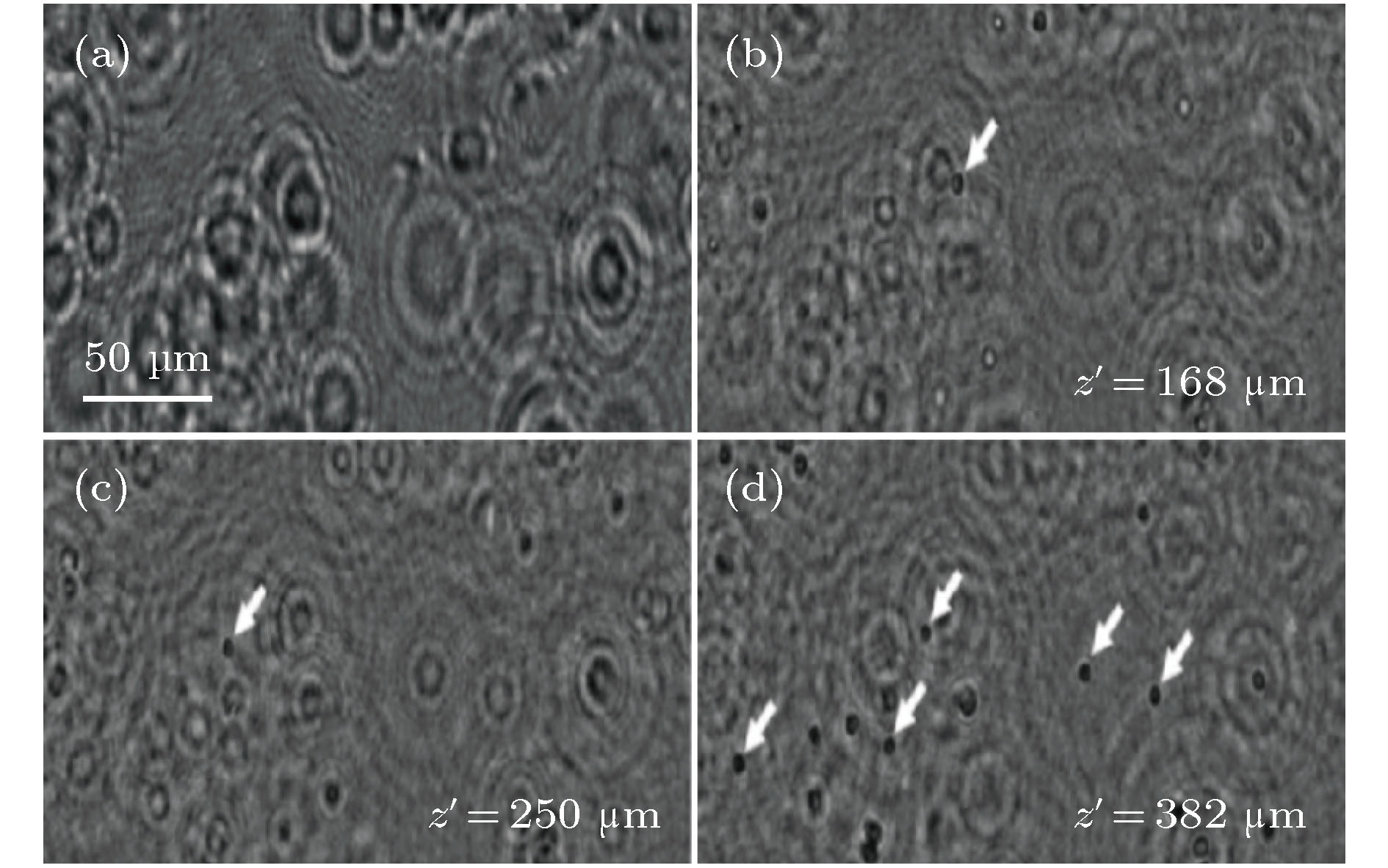
图 6 RBC的全息图与重建图像 (a) CMOS像感器拍摄FEP微管内RBC所得全息图; (b), (c), (d)分别表示不同重建深度下RBC重建图像, 箭头表示聚焦的RBC[51]
Fig. 6. The hologram and the reconstruction images of RBCs. (a) The RBC hologram obtained from CMOS; (b), (c), and (d) represent RBC reconstruction images at different reconstruction depths, respectively. Each focused RBC is shown by an arrow[51].
图 8 RBC的相位重建图像 (a)重建的口腔形状RBC相位图像; (b)重建的盘状RBC相位图像; (c)重建后经分水岭算法分割的口腔形状RBC相位图像; (d)重建后经分水岭算法分割的盘状RBC相位图像; (e)分割的单个RBC相位图像; (f)(g)(h)分别经标记分水岭算法进一步分割得到的单个RBC的A、B、C部分[54]
Fig. 8. The reconstructed phase image for RBCs (a) The reconstructed phase image for RBCs having a stomatocyte shape; (b) the reconstructed RBCs phase image for RBCs having a discocyte shape; (c)the segmented phase image for RBCs having a stomatocyte shape; (d) the segmented phase image for RBCs having a discocyte shape; (e) the segmented phase image for single RBC(f), (g) and (h) represent the A, B and C parts by the marker-controlled watershed algorithm in RBC, respectively[54].
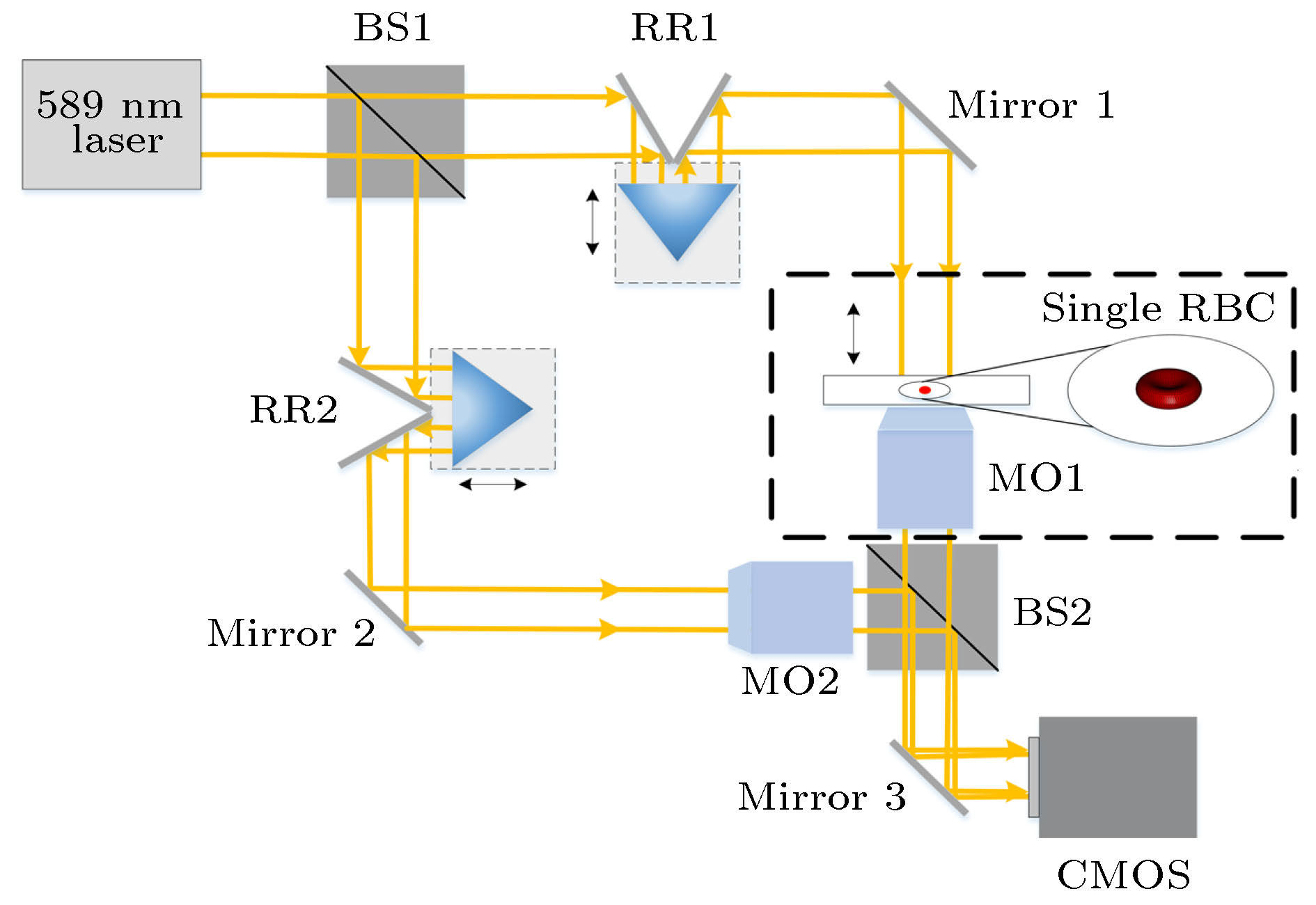
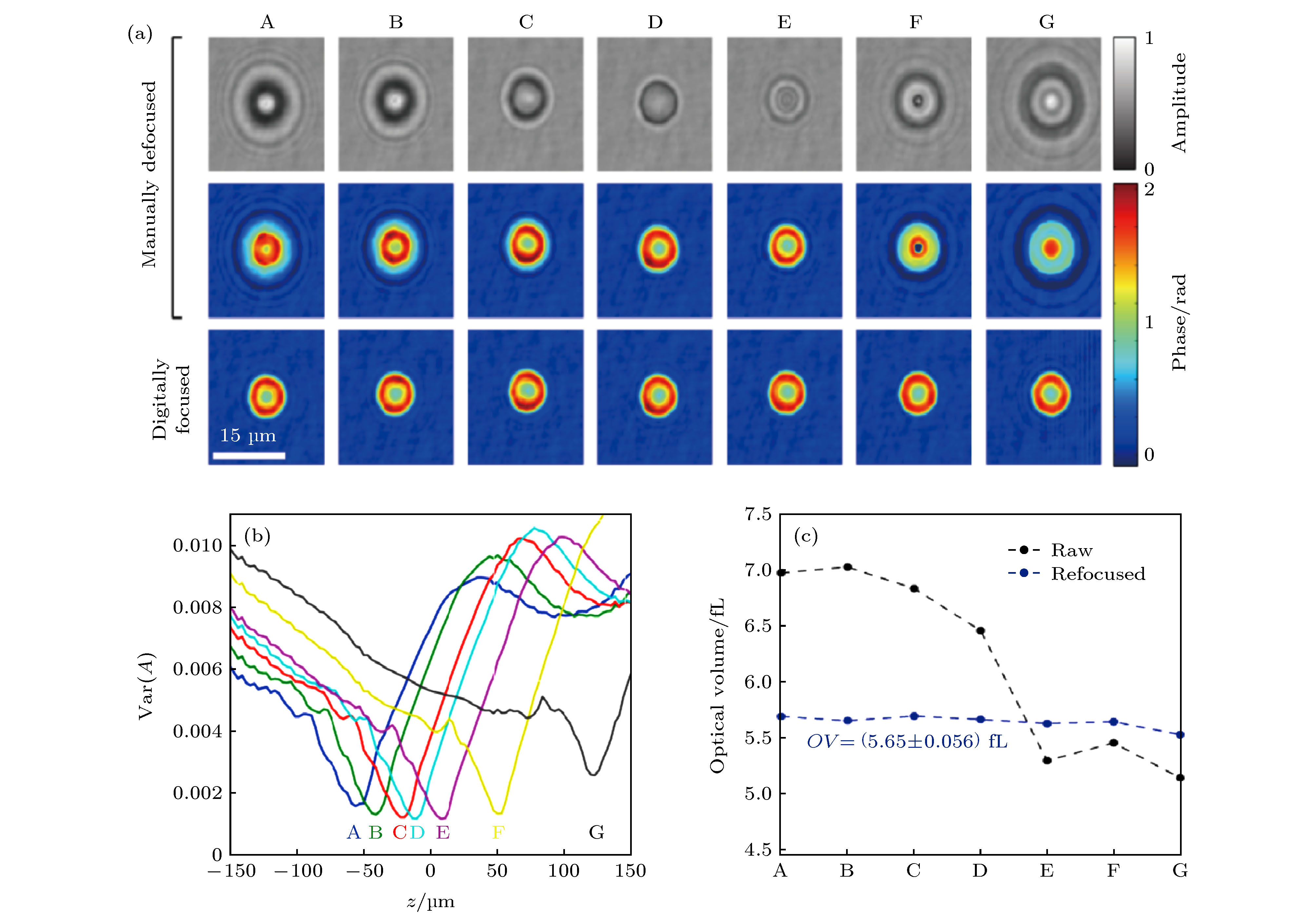
图 10 对单一RBC图像进行数字重聚焦与相应的RBC光学体积测量 (a)通过人工聚焦方法与数字重聚焦方法对单一RBC重建所得振幅图与相位图; (b)A—G的振幅方差分布; (c)RBC在人工聚焦方法所得光学体积(黑线)与数字重聚焦方法所得光学体积(蓝线), 光学体积OV表示为平均值 ± 标准差[53]
Fig. 10. Digital refocusing of a single red blood cell image and corresponding optical volume measurements. (a) The amplitude and phase images by the manually-focused method and digitally-refocused method from a single RBC; (b) amplitude variance metric of holograms A-G; (c) computed OV of RBC from manually-focused phase images(black) and digitally-refocused phase images(blue). OV reported as mean ± standard deviation[53].
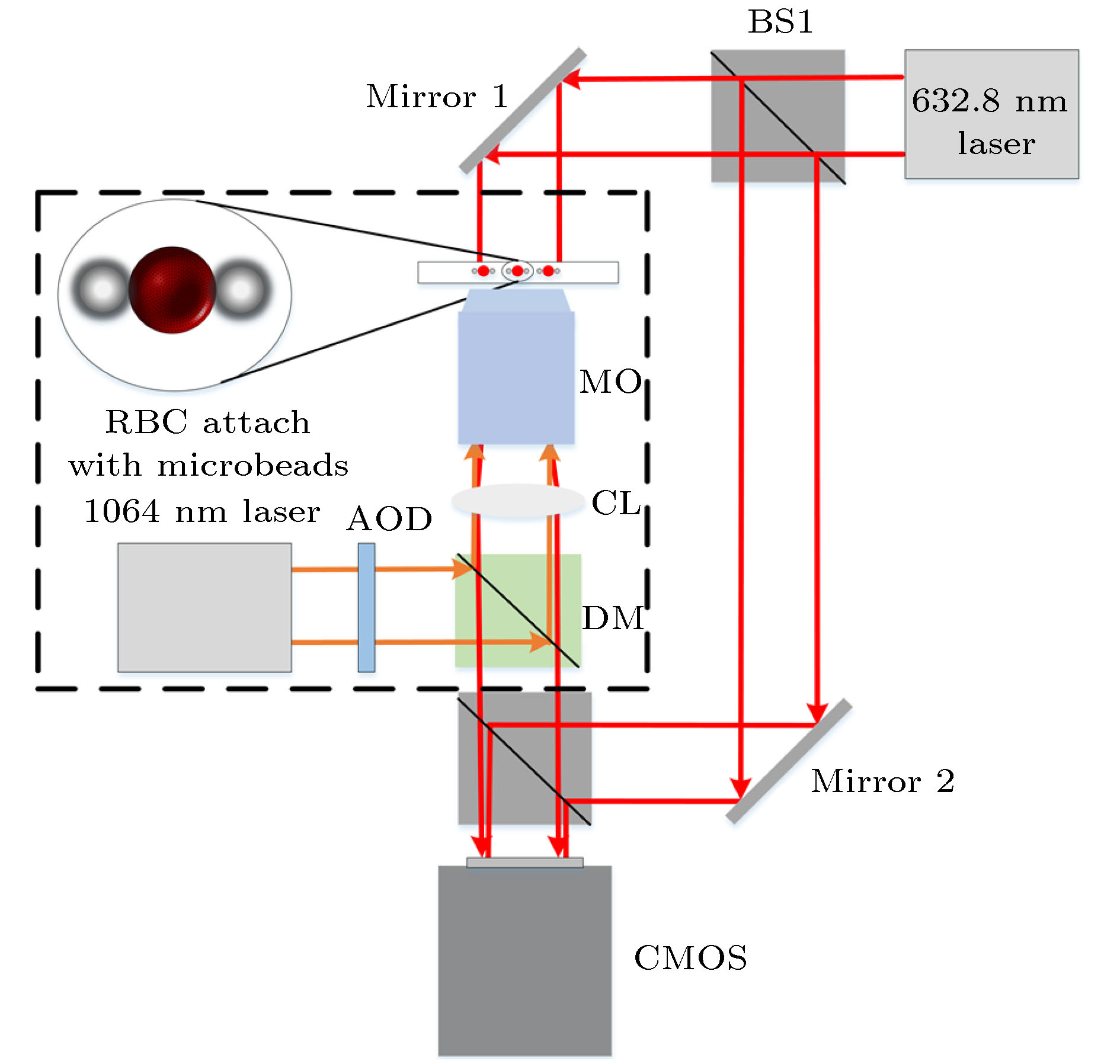
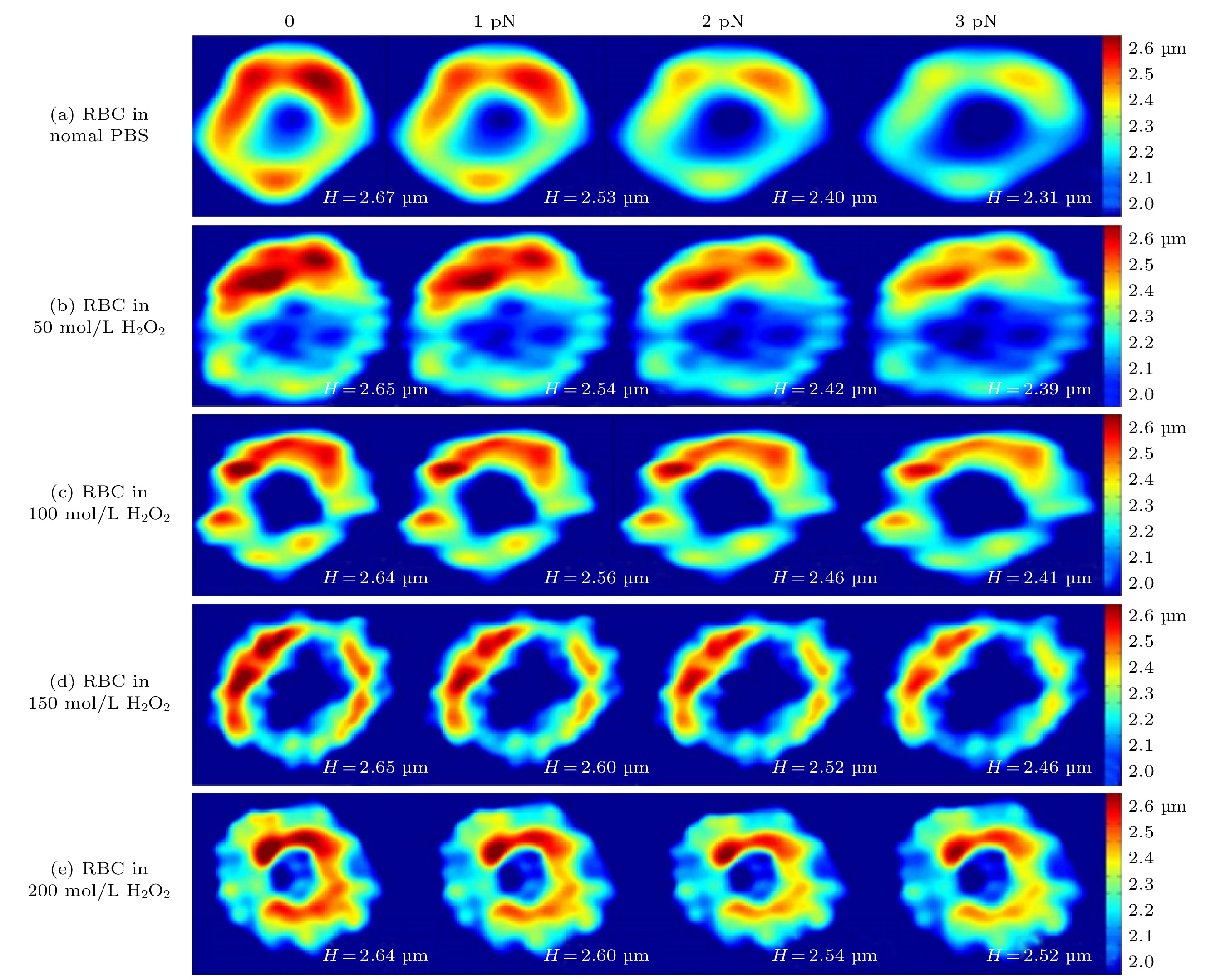
图 12 0−3 pN陷阱拉伸力变化下不同浓度(0−200 μmol/L)氧化应激下重建RBC的高度变化, 颜色深浅代表RBC高度的大小[72]
Fig. 12. Height change of reconstructed RBCs under different concentrations of oxidative stress (0−200 μmol/L). Four images in each group are corresponding to trap force varying from 0−3 pN. Color bar represents different thickness[72].
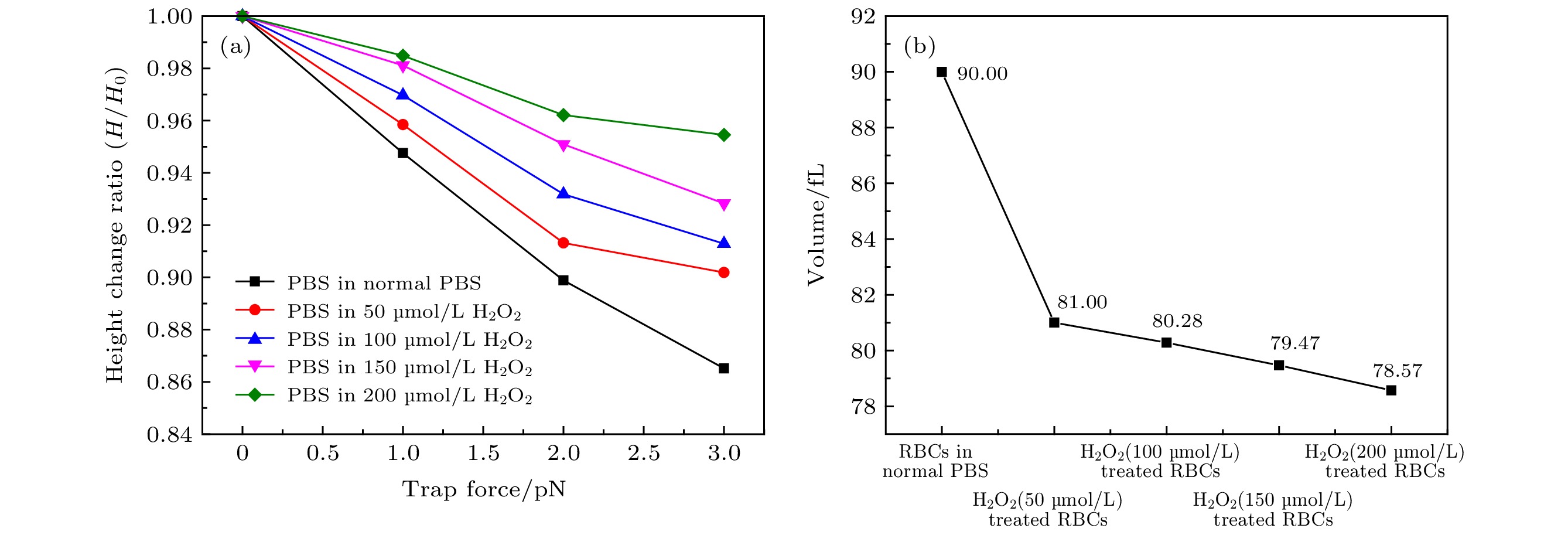
图 13 RBC在不同浓度氧化应激下的性能 (a)不同浓度氧化应激下RBC最大高度H与陷阱拉伸力关系; (b)不同浓度氧化应激下RBC体积[72]
Fig. 13. Performance of RBC under different oxidative stress. (a) The relationship between the maximum height H of RBC and the trap tensile force under different oxidative stress; (b) the volume of RBC under different oxidative stress[72].
坐标 测量精度/μm 均方根误差/μm $x$ ± 0.3 0.63 $y$ ± 0.3 0.52 $z$ ± 1.0 2.05 表 2 两种不同形状RBC的A、B部分的三维体积
Table 2. The different shapes of RBC’s three-dimensional volume of A and B parts.
A部分 B部分 平均体积/μm3 均方根
误差平均体积/μm3 均方根
误差口腔状 7.6 7.2 41.5 14.7 盘状 14.6 8.0 32.7 7.3 -
[1] Cuche E, Marquet P, Depeursinge C 1999 Appl. Opt. 38 6994
 Google Scholar
Google Scholar
[2] Ferraro P, Coppola G, De Nicola S, Finizio A, Pierattini G 2003 Opt. Lett. 28 1257
 Google Scholar
Google Scholar
[3] Ferraro P, Miccio L, Grilli S, Paturzo M, De Nicola S, Finizio A, Osellame R, Laporta P 2007 Opt. Express 15 14591
 Google Scholar
Google Scholar
[4] Charrière F, Marian A, Montfort F, Kuehn J, Colomb T, Cuche E, Marquet P, Depeursinge C 2006 Opt. Lett. 31 178
 Google Scholar
Google Scholar
[5] Kemper B, Von Bally G 2008 Appl. Opt. 47 A52
 Google Scholar
Google Scholar
[6] Potcoava M, Kim M 2008 Meas Sci Technol 19 074010
 Google Scholar
Google Scholar
[7] 袁操今, 翟宏琛 2010 光子学报 39 893
 Google Scholar
Google Scholar
Yuan C J, Zhai H C 2010 Acta Phot. Sin. 39 893
 Google Scholar
Google Scholar
[8] Ma J, Yuan C, Situ G, Pedrini G, Osten W 2013 Chin. Opt. Lett. 11 090901
 Google Scholar
Google Scholar
[9] 王华英, 刘飞飞, 成惠, 廖薇, 赵宝群, 于梦杰, 刘佐强 2013 强激光与粒子束 25 345
 Google Scholar
Google Scholar
Wang H Y, Liu F F, Cheng H, Liao W, Zhao B Q, Yu M J, Liu Z Q 2013 High Pow Las Part Beam 25 345
 Google Scholar
Google Scholar
[10] 王华英, 刘飞飞, 宋修法, 廖微, 赵宝群, 于梦杰, 刘佐强 2013 物理学报 62 024207
 Google Scholar
Google Scholar
Wang H Y, Liu F F, Liao W, Song X F, Yu M J, Liu Z Q 2013 Acta Phys. Sin. 62 024207
 Google Scholar
Google Scholar
[11] Zheng J, Pedrini G, Gao P, Yao B, Osten W 2015 J. Opt. 17 085301
 Google Scholar
Google Scholar
[12] Lin Q, Wang D, Wang Y, Rong L, Chang S 2015 Opt. Lasers Eng. 66 279
 Google Scholar
Google Scholar
[13] Wang Y, Guo S, Wang D, Lin Q, Rong L, Zhao J 2016 Opt. Commun. 366 81
 Google Scholar
Google Scholar
[14] 董可平, 钱晓凡, 张磊, 张永安 2007 光子学报 36 2013
Dong K P, Qian X F, Zhang L, Zhang Y A 2007 Acta Phot. Sin. 36 2013
[15] 邸江磊, 赵建林, 范琦, 姜宏振, 孙伟伟 2008 光学学报 28 56
 Google Scholar
Google Scholar
Di J L, Zhao J L, Fan Q, Jiang H Z, Sun W W 2008 Acta Optic. Sin. 28 56
 Google Scholar
Google Scholar
[16] 马利红, 王辉, 金洪震, 李勇 2012 中国激光 39 215
Ma L H, Wang H, Jin H Z, Li Y 2012 Chin. J. Las. 39 215
[17] Cao R, Xiao W, Wu X, Sun L, Pan F 2018 Biomed. Opt. Express 9 72
 Google Scholar
Google Scholar
[18] Zhang J, Chen Q, Sun J, Zuo C 2019 Seventh International Conference on Optical and Photonic Engineering (icOPEN 2019), Phuket, Thailand, October 16, 2019 p112050 C
[19] Zhang J, Sun J, Chen Q, Zuo C 2020 IEEE Trans. Comput. Imaging. 6 697
 Google Scholar
Google Scholar
[20] Amos W, White J 2003 Biol. Cell 95 335
 Google Scholar
Google Scholar
[21] Subramaniam V, Kirsch A, Jovin T 1998 Cell. Mol. Biol. (Noisy-le-grand) 44 689
[22] Huang D, Swanson E A, Lin C P, Schuman J S, Stinson W G, Chang W, Hee M R, Flotte T, Gregory K, Puliafito C A 1991 Science 254 1178
 Google Scholar
Google Scholar
[23] Kemper B, Carl D, Knoche S, Thien R, von Bally G 2004 Optical Metrology in Production Engineering Strasbourg, France, September 10, 2004 p581
[24] Jin H, Wan H, Zhang Y, Li Y, Qiu P 2008 J. Mod. Opt. 55 2989
 Google Scholar
Google Scholar
[25] 周海宪 2006 应用光学 27 I0007
Zhou H X 2006 J. Appl. Opt. 27 I0007
[26] Nehmetallah G T, Aylo R, Williams L 2015 Analog and Digital Holography with MATLAB (Bellingham: Society of Photo-Optical Instrumentation Engineers (SPIE)) pp137–143
[27] Kreis T M, Adams M, Jüptner W P 1997 Optical Inspection and Micromeasurements II Munich, Germany, September 17, 1997 p224
[28] Liu C, Wang D, Zhang Y 2009 Opt. Eng. 48 105802
 Google Scholar
Google Scholar
[29] Song X, Zhao B, Qin A 4th International Symposium on Advanced Optical Manufacturing Chengdu, China, November 19−21, 2008 p728340
[30] Huaying W, Baoqun Z, Wei L 2009 IEEE International Conference on Intelligent Computing and Intelligent Systems, Shanghai, China, November 20−22, 2009 p838
[31] 王广俊, 王大勇, 王华英 2010 激光与光电子学进展 47 030901
 Google Scholar
Google Scholar
Wang G J, Wang D Y, Wang H Y 2010 Laser Optoelectron. Prog. 47 030901
 Google Scholar
Google Scholar
[32] Goodman J W 2005 Introduction To Fourier Optics (Placerville: Roberts and Company Publishers) pp298–306
[33] Lai S, King B, Neifeld M A 2000 Opt. Commun. 173 155
 Google Scholar
Google Scholar
[34] Yamaguchi I, Zhang T 1997 Opt. Lett. 22 1268
 Google Scholar
Google Scholar
[35] Kim M-K 2010 J. Opt. Soc. Korea 14 77
 Google Scholar
Google Scholar
[36] Colomb T, Cuche E, Charrière F, Kühn J, Aspert N, Montfort F, Marquet P, Depeursinge C 2006 Appl. Opt. 45 851
 Google Scholar
Google Scholar
[37] 惠梅, 王东生, 李庆祥, 邓年茂, 徐毓娴 2003 光学学报 23 1245
 Google Scholar
Google Scholar
Hui M, Wang D S, Li Q X, Deng N M, Xu Y X 2003 Acta Optic. Sin. 23 1245
 Google Scholar
Google Scholar
[38] 葛宝臻, 崔鹏, 吕且妮, 魏耀林 2008 中国石油大学学报: 自然科学版 32 169
Ge B Z, Cui P, Lv Q N, Wei Y L 2008 J. China U. Pet.: Nat. Sci. Ed. 32 169
[39] 朱娜娜, 金孝岠, 郭建荣 2019 中国糖尿病杂志 27 12
Zhu N N, Jin X J, Guo J R 2019 Chin. J. Diabetes Mellitus 27 12
[40] Lee S, Park H, Kim K, Sohn Y, Jang S, Park Y 2017 Sci. Rep. 7 1
 Google Scholar
Google Scholar
[41] 丁宁, 陈长强, 樊绮诗 2019 检验医学 34 889
Ding N, Chen C Q, Fan Q S 2019 Lab. Med. 34 889
[42] Li N, Zhou H, Tang Q 2017 Dis. Markers 2017 1
[43] Jenner P 2003 Ann. Neurol. 53 S26
 Google Scholar
Google Scholar
[44] Hald A, Lotharius J 2005 Exp. Neurol. 193 279
 Google Scholar
Google Scholar
[45] Spirito P, Maron B J, Bonow R O 1986 J. Am. Coll. Cardiol. 7 518
 Google Scholar
Google Scholar
[46] Harders A G, Gilsbach J M 1987 J. Neurosurg. 66 718
 Google Scholar
Google Scholar
[47] Sugii Y, Okuda R, Okamoto K, Madarame H 2005 Meas. Sci. Technol. 16 1126
 Google Scholar
Google Scholar
[48] Lima R, Wada S, Takeda M, Tsubota K-i, Yamaguchi T 2007 J. Biomech. 40 2752
 Google Scholar
Google Scholar
[49] Jia Y, Morrison J C, Tokayer J, Tan O, Lombardi L, Baumann B, Lu C D, Choi W, Fujimoto J G, Huang D 2012 Biomed. Opt. Express 3 3127
 Google Scholar
Google Scholar
[50] van den Berg P, Daoudi K, Steenbergen W 2015 Photoacoustics 3 89
 Google Scholar
Google Scholar
[51] Choi Y S, Lee S J 2009 Appl. Opt. 48 2983
 Google Scholar
Google Scholar
[52] Zakrisson J, Schedin S, Andersson M 2015 Appl. Opt. 54 7442
 Google Scholar
Google Scholar
[53] Rinehart M T, Park H S, Wax A 2015 Biomed. Opt. Express 6 2067
 Google Scholar
Google Scholar
[54] Yi F, Lee C-G, Moon I-K 2012 J. Opt. Soc. Korea 16 115
 Google Scholar
Google Scholar
[55] Fällman E, Schedin S, Jass J, Andersson M, Uhlin B E, Axner O 2004 Biosens. Bioelectron. 19 1429
 Google Scholar
Google Scholar
[56] Andersson M, Fällman E, Uhlin B E, Axner O 2006 Biophys. J. 91 2717
 Google Scholar
Google Scholar
[57] Groen F C, Young I T, Ligthart G 1985 Cytometry A 6 81
 Google Scholar
Google Scholar
[58] Sheng J, Malkiel E, Katz J 2006 Appl. Opt. 45 3893
 Google Scholar
Google Scholar
[59] Langehanenberg P, Kemper B, Dirksen D, Von Bally G 2008 Appl. Opt. 47 D176
 Google Scholar
Google Scholar
[60] Moon I, Daneshpanah M, Javidi B, Stern A 2009 Proc. IEEE Inst. Electr. Electron Eng. 97 990
 Google Scholar
Google Scholar
[61] Moon I, Javidi B, Yi F, Boss D, Marquet P 2012 Opt. Express 20 10295
 Google Scholar
Google Scholar
[62] Gonzalez R, Woods R E 2002 Digital Image Processing (New York: Prentice-Hall) pp588−596
[63] Rencher A C 1998 Multivariate Statistical Inference and Applications (New York: Wiley) pp41−63
[64] Masters B R 2012 J. Biomed. Opt. 17 029901
 Google Scholar
Google Scholar
[65] Mir M, Wang Z, Shen Z, Bednarz M, Bashir R, Golding I, Prasanth S G, Popescu G 2011 P NATL ACAD SCI USA 108 13124
 Google Scholar
Google Scholar
[66] Shaked N T, Finan J D, Guilak F, Wax A P 2010 J Biomed Opt 15 010505
 Google Scholar
Google Scholar
[67] Park Y, Diez-Silva M, Popescu G, Lykotrafitis G, Choi W, Feld M S, Suresh S 2008 Proc. Natl. Acad. Sci. 105 13730
 Google Scholar
Google Scholar
[68] Dubois F, Schockaert C, Callens N, Yourassowsky C 2006 Opt. Express 14 5895
 Google Scholar
Google Scholar
[69] Xu L, Mater M, Ni J 2011 Opt. Express 19 14779
 Google Scholar
Google Scholar
[70] Liebling M, Unser M 2004 J. Opt. Soc. Am. A. Opt. Image. Sci. Vis. 21 2424
 Google Scholar
Google Scholar
[71] Hwang O 2013 Exp. Neurobiol. 22 11
 Google Scholar
Google Scholar
[72] Liu J, Zhu L, Zhang F, Dong M, Qu X 2019 Appl. Opt. 58 4042
 Google Scholar
Google Scholar
[73] Felgner H, Müller O, Schliwa M 1995 Appl. Opt. 34 977
 Google Scholar
Google Scholar
[74] Florin E-L, Pralle A, Stelzer E, Hörber J 1998 Appl. Phys. A 66 S75
 Google Scholar
Google Scholar
[75] Schlenker T, Feranchak A P, Schwake L, Stremmel W, Roman R M, Fitz J G 2000 Gastroenterology 118 395
 Google Scholar
Google Scholar
计量
- 文章访问数: 18384
- PDF下载量: 480
- 被引次数: 0












 下载:
下载: